近年来,在国内医药市场加速改革的机遇下,复宏汉霖(02696)依托自身强劲的研发实力,辅以外部合作引进,以“内外兼修”的姿态全面加速创新,取得了一定成果,并获香港联交所批准于今年4月23日起股票代码可摘除标记“B”。
2021年4月22日,复宏汉霖宣布,公司自主研制的创新型PD-1抑制剂HLX10(斯鲁利单抗)针对MSI-H实体瘤适应症的NDA正式获国家药监局NMPA受理并拟纳入优先审评审批。这一消息引发了业界及市场的广泛关注。
而在复宏汉霖不久前公布的一项斯鲁利单抗单药治疗高度微卫星不稳定型或错配修复缺陷型(MSI-H/dMMR)实体瘤的2期关键临床研究中,斯鲁利单抗已展现出对MSI-H实体瘤适应症良好的疗效和安全性。
智通财经APP了解到,高度微卫星畸变常发生在多个癌种中,如子宫内膜癌、结直肠癌、胃癌、肾细胞癌及卵巢癌等,有研究显示MSI-H在所有癌种中的发生率约为14%,MSI-H也已逐渐成为预测实体瘤患者免疫治疗效果的重要生物标志物。然而国内的PD-1单抗虽竞相上市,但尚未有批准用于MSI-H / dMMR晚期实体瘤的抗PD-1单抗,庞大的治疗需求远未被满足。在此背景下,复宏汉霖依托“Combo + Global”战略自主研发的斯鲁利单抗就显现出其差异化优势。
实际上,在汉利康和汉曲优两款产品商业化步入正轨后,复宏汉霖已形成从创新研发到产品商业化的完备产业链体系,斯鲁利单抗仅是其创新管线中的一个缩影。目前,斯鲁利单抗已成为复宏汉霖的创新先导产品,在公司国际商业化能力加持下,其开发潜力值得期待。
“联合疗法+大瘤种覆盖”探寻PD-1最后一片蓝海
从最初比拼临床开发进度,到后期比拼上市和产能扩张速度,再到如今比拼价格,国内围绕PD-1的市场争夺战正愈演愈烈。然而在PD-1市场以价换量、不断压低边际成本的背后,差异化的开发就成了“破圈”的关键方向。
智通财经APP了解到,在细分患者群体中,如PD-L1阳性、TMB(肿瘤突变负荷)高、MSI-H(微卫星不稳定性高)等生物标志物检测呈阳性的患者中,他们通常对于免疫检查点抑制剂有较高的应答率,因为抗PD-(L)1产品单独用药疗效较好。
但是在大多数未进行标志物检测的实体瘤患者中,PD-1/L1的整体有效率仍然较低。根据Embase、PubMed和Cochrane数据库中截至2019年7月关于国外6种抗PD-(L)1单抗单药治疗的前瞻性临床试验,来自针对26种癌症的160项试验的22165例患者的总体平均客观缓解率只有20.21%。
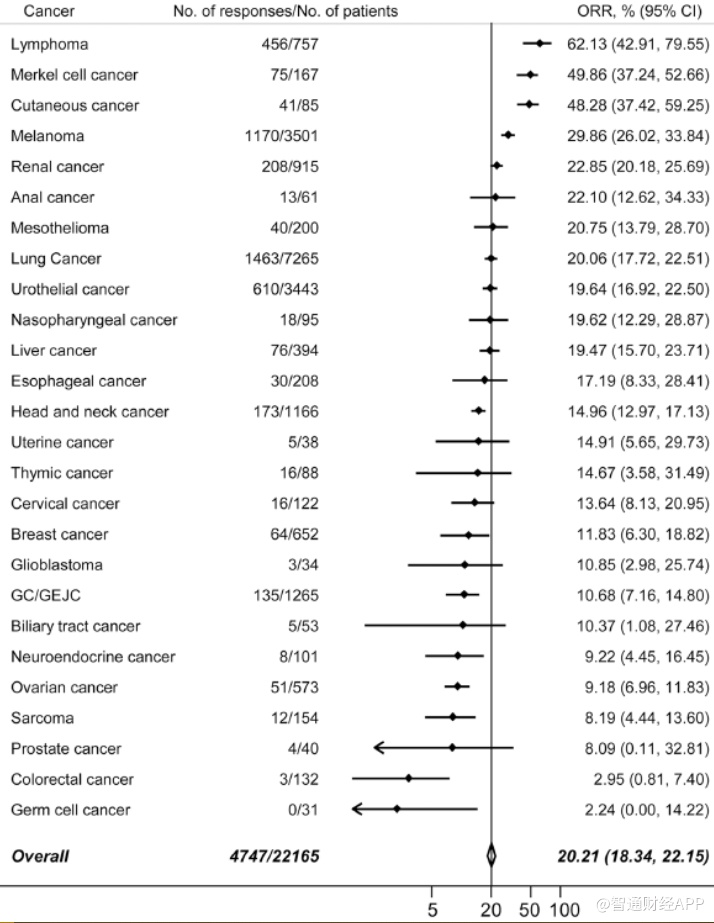
可见,仅从单药适应症角度考量,受制于治疗效果等因素,国际上现有PD-1药物的应用场景实际较为有限。所以,联合疗法与适应症的全面覆盖便成为PD-1的突围方向。
也正是因此,虽然国内市场上PD-1的竞争已经较为激烈,但复宏汉霖的PD-1单抗仍很有看点。
据悉,在复宏汉霖的成熟的创新研发平台支持下,斯鲁利单抗已快速推进各种免疫联合疗法的开发并拓宽治疗领域。目前,斯鲁利单抗共有10项免疫肿瘤疗法临床试验正在进行中,其适应症全面覆盖高度微卫星不稳定型实体瘤(MSI-H)、肺癌、肝细胞癌、食管癌、头颈癌、胃癌等国内主要瘤种,且在多个实体瘤适应症上进行到了III期临床研究阶段。且针对国际上研究较少的鳞状非小细胞肺癌和小细胞肺癌,复宏汉霖也差异化地启动了国际多中心临床研究,目前皆在III期临床开发阶段,开展的3项肺癌适应症的研究可覆盖至超过90%的肺癌患者。继MSI-H之后,复宏汉霖同步计划于2021年下半年向NMPA递交斯鲁利单抗一线治疗鳞状非小细胞肺癌的上市注册申请。
除了不断覆盖更多适应症尤其是关键大瘤种外,复宏汉霖还在积极探索联合疗法,通过“1+1>2”的方式为患者提供更优的治疗解决方案。据智通财经APP了解,围绕斯鲁利单抗这一免疫治疗的核心产品,公司在国内率先开展了联合治疗研究,目前围绕斯鲁利单抗为核心已开展了8项联合治疗方案,均已进入2/3期后期临床阶段。
关于斯鲁利单抗的联合疗法开发,业界和市场一直保持高度关注,原因在于其展示出的良好的治疗特性及潜在的社会经济性。
以斯鲁利单抗和贝伐珠单抗HLX04联合疗法为例,从疗效上看,靶向VEGF的贝伐珠单抗本身具有抗血管生成作用,不仅对肿瘤血管生成和癌细胞的增殖有直接影响,还能增强肿瘤的免疫原性、T细胞的浸润等。这一特性让HLX04与斯鲁利单抗单抗联用时,能够增强活化T细胞对肿瘤抗原的应答,进一步增强杀灭癌细胞的能力。
从社会经济性来看,抗体研发、生产成本往往较高,即便是发达国家的患者也难以负担。HLX04与斯鲁利单抗联合疗法的相对优势在于,两款产品均为复宏汉霖单抗创新药产品管线中极具代表性的免疫治疗抗体产品,公司能够通过对研发、生产成本的严格把控,将肿瘤免疫联合疗法费用控制到更低,大幅度提高患者的可负担性,从而促进联合治疗的普及化。
此外,对于公司而言,联合自主产品进行联合疗法的开发,也能节约产品的引入成本,提高公司的利润空间。
以上不难看出,复宏汉霖大瘤种覆盖及联合疗法的开发策略成果显著,为不占速度先机的斯鲁利单抗奠定了差异化优势。
从MSI-H实体瘤适应症看斯鲁利单抗开发潜力
从复宏汉霖本次获得NDA受理的MSI-H实体瘤适应症来看,本次递交主要依据一项在单药治疗经标准治疗失败的,不可切除或转移性高度微卫星不稳定型或错配修复缺陷型(MSI-H / dMMR)实体瘤中开展的关键2期临床研究结果,公司近期宣布该研究已达到主要终点。且该项临床研究的结果证明了斯鲁利单抗在此类适应症中具有良好的疗效和安全性。
智通财经APP了解到,MSI-H实体瘤是指一类具有微卫星高度不稳定(MSI-H)表型的实体瘤,最早在遗传性结直肠癌中被发现,此后研究发现,MSI普遍存在于其他癌症类型患者中,其中包括子宫内膜癌,胃癌,肝细胞癌,黑色素瘤等癌细胞中。由于不依据病灶部位而参考肿瘤标志物检测进行划分,变相增加了产品开发难度。
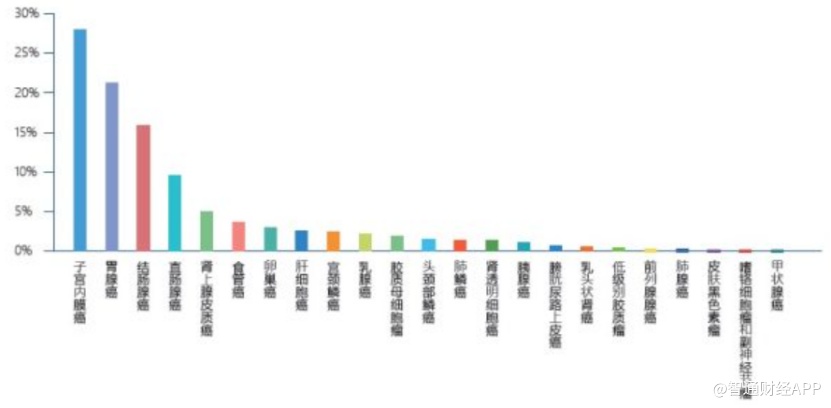
据统计,早在2015年中国便有约430万癌症新发病例,而根据国家癌症中心的《中国恶性肿瘤流行情况分析报告》各肿瘤的发病率及JCO Precis Oncol对各癌种MSI-H发生率的测算,国内一些常见癌种中每年新发MSI-H的实体瘤患者数量约为31.2万人,与每年新发乳腺癌病例数相当,且远远超过前列腺癌、甲状腺癌、卵巢癌、淋巴瘤等,其适应症市场开发潜力值得期待。
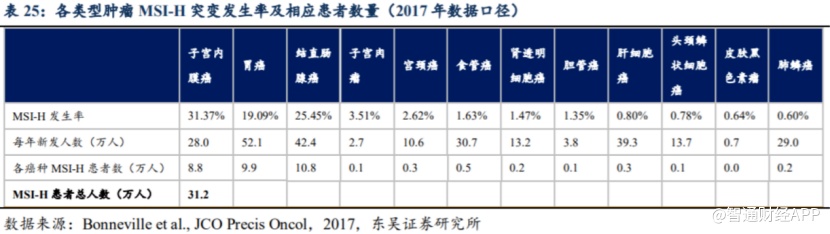
然而,面对国内日益增长的未满足治疗需求,国内尚未有相关适应症产品获批。在此背景下,作为国内首款应用于PD-1高度微卫星不稳定型实体瘤适应症的产品,斯鲁利单抗值得市场高度关注。
以MSI-H/dMMR实体瘤适应症患者总数31.2万、药物治疗MSI-H肿瘤患者比例60%及产品渗透率18%计算,预计2030年,MSI-H/dMMR实体瘤潜在用药人群预计达到18.7万人。
而基于复宏汉霖出色的国际商业化能力,公司也有望将产品放量发展的上限拉到更广阔的国际市场高度。在国内PD-1产品暗中较量,战火不断升级的当下,出海或将成为一条明智之路。
国际商业化实力支撑PD-1“出海”
复宏汉霖创新研发成果高效转化为国际商业化能力的第一步,在于建立一套可靠的生产体系及国际化的质量管理体系。高标准的国际化质量管理体系以及强有力的产能支撑,为复宏汉霖把握国际商业化先发优势打下坚实基础。
据智通财经APP了解,2020年以来,为满足持续增长的市场需求,复宏汉霖积极推动了生产规模的提升,完成500L向2000L的生产设备扩容。公司徐汇基地现拥有10个2000L的大规模一次性生物反应器,整体可使用商业化产能已提升至20000L。产能的大幅扩增,为公司重磅产品的销售快速增长奠定了坚实的基础。
在质量管理体系方面,近年来,徐汇基地及配套的质量管理体系已通过由中国国家药品监督管理局(NMPA)、欧洲药品管理局(EMA)、欧盟质量受权人(QP)以及国际商业合作伙伴进行的多项实地核查及审计,并获得了中国与欧盟GMP认证,由此成为了国内首个获得欧盟GMP认证用于生产自主研发抗体生物药的GMP工厂。
公司也在同步扩大松江基地的产能建设,松江基地(一)计划建设产能24000L,已于开始进行临床样品的GMP生产,并不断优化平台优势和连续化生产等先进生产技术的应用,以技术创新带动产能增加和成本下降。松江基地(二)一期项目主要生产楼预计将于2021年完工投入试生产并开展相关验证工作。
而在国产PD-1产品竞相出海的新阶段,作为国内生物药领域的龙头公司,复宏汉霖在国际商业化布局上历经的多年沉淀和优势积累,或将助力公司在PD-1领域实现“弯道超车”。
在产品的国际化研发方面,复宏汉霖在海外的药政注册能力、临床开发和运营能力可支持公司在全球多个地区开展临床试验。就斯鲁利单抗而言,该产品除在国内递交上市申请外,目前也同步在美国及欧盟等国家和地区获得临床试验许可,并于中国、土耳其、波兰、乌克兰、俄罗斯等国家及地区累计入组约2000名患者,成为拥有国际临床数据较多的PD-1产品之一。
在国际商业化方面,早在2019年,复宏汉霖就KG Bio达成合作共识,授予KG Bio关于斯鲁利单抗的首个单药疗法及两项联合疗法在东南亚地区10个国家的独家开发和商业化权利。借助该分销渠道,公司有望加快斯鲁利单抗在东南亚地区市场拓展的步伐,并为后续为进入更广阔的国际市场奠定基础,惠及全球更多病患。
值得一提的是,复宏汉霖的自身研发实力还是有目共睹的,公司目前已上市的3款产品皆通过依赖自身研发实力自主开发。而就公司当前阶段的发展策略来说,同时强调辅以外部合作引进,“内外兼修”全面加速创新,以PD-1为先导加快推进生物创新药的开发,进而覆盖多个创新靶点。
除了斯鲁利单抗已取得了显著的进展外,目前复宏汉霖创新产品管线中还有超过20款候选药物在研,全面覆盖HER2、VEGF、EGFR、PD-1、PD-L1、c-MET、DR4、S1 Protein of SARS-CoV-2等靶点。并且公司还在同步优化单抗/双抗平台,积极开展创新靶点、双特异性抗体、ADC等产品的布局,持续推动早期项目储备。

在创新产品的引进上,复宏汉霖近期也动作频繁,2021年初,复宏汉霖向日本Chiome公司引入抗TROP2抗体及相关知识产权在中国的研究、开发、生产和商业化的独家权利,探索该产品在在多种实体瘤中的广谱疗效,就ADC、双特异性抗体、组合疗法等领域进行全面开发。3月,复宏汉霖进一步拓展靶点布局,首次引入小分子抑制剂RX208(BRAF V600E抑制剂),向Best-in-Class的产品发出冲击。
今年4月20日,复宏汉霖宣布,公司已通过港交所上市规则第8.05(3)条下的市值/收益测试,符合在港股生物科技板块之外上市的要求。经港交所批准后,复宏汉霖将于2021年4月23日起将“B”标志从股票代码中移除,这也就意味着复宏汉霖成为了港股生物技术板块中继百济神州、信达生物和君实生物之后第4家实现股票代码成功摘“B”的公司,此次顺利摘B也体现出市场对于复宏汉霖产品商业化后业绩逐步提高的认可。
综上所述,在多年积累的差异化创新及国际商业化优势下,复宏汉霖已拥有了覆盖抗体药物开发全流程的创新研发及商业化能力。伴随着汉利康、汉曲优等新品的陆续获批上市及其他在研新药向前推进,公司在进入全面加速创新的发展阶段同时,也得到了资本市场的认可。
作为复宏汉霖单抗创新药产品管线中的先导产品,斯鲁利单抗可谓身负厚望,有备而来。随着斯鲁利单抗商业化号角的吹响,也再次向市场证明了公司持续性的产业化开发能力,继汉利康、汉曲优等重磅产品顺利商业化后,未来斯鲁利单抗的获批和发布无疑能带来额外的收入机会,继续推动复宏汉霖作为一家生物技术公司持续成长,为公司未来估值稳定上升打下牢固基础。






