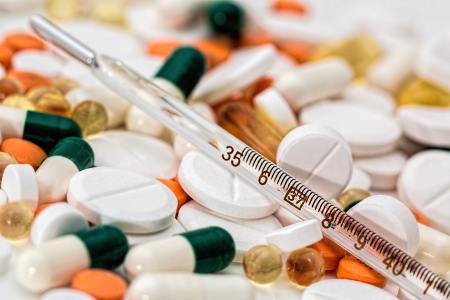
本文来自微信公众号“医药观澜”。
截止2021年3月20日,中国国家药监局药品审评中心(CDE)数据显示,共计有3982项临床试验申请通过“默示许可”。本周新增47项临床试验默示许可,其中有21项1类创新药申请(不含补充申请),涉及14款药物,包括RNAi疗法、GLP-1受体激动剂、ROS1和NTRK双靶点小分子抑制剂等等。本文将分享其中部分获批临床的新药信息,仅供读者参阅(排名不分先后)。

1、Dicerna/罗氏(Roche):RO7445482注射液
适应症:慢性乙型肝炎
公开资料显示,目前乙肝难于治愈的原因是HBV能够在被感染细胞的细胞核中生成共价闭合环状DNA(cccDNA)和整合序列。这些序列的半衰期非常长,目前的标准疗法不能有效清除cccDNA。RO7445482能够生成一款靶向HBV基因组特定区域的RNAi,它能够特异性敲低HBV mRNA的生成和HBV进入细胞所需的基因。 2020年11月,Dicerna公司公布了RO7445482治疗慢性乙型肝炎的1期临床试验结果。在该研究中,18名服用核苷(酸)抗病毒疗法的慢性乙肝患者在背景疗法基础上,分别接受不同剂量的RO7445482或安慰剂的治疗。试验结果显示:每月一次,总计4次的RO7445482治疗导致HBV疾病活动生物标志物的大幅和持久降低;最后一次给药后乙肝表面抗原(HBsAg)水平持续降低时间可长达1年。 2、辉瑞(Pfizer):PF-06882961片 适应症:用于2型糖尿病患者控制血糖 Danuglipron(PF-06882961)是一款口服小分子GLP-1受体激动剂。GLP-1受体激动剂的开发已经有不短的历史,目前已经上市的许多GLP-1类似物都在帮助糖尿病患者降低血糖方面取得良好的疗效。然而,这些多肽类药物通常需要患者通过注射接受治疗。据介绍,辉瑞开发的danuglipron具有多种潜在优点,包括能够实现血糖和体重的有效控制、耐受性良好、口服剂型方便使用、生物利用度高等等。 在1期临床试验中,接受danuglipron治疗的2型糖尿病患者在服药四周后,空腹血糖水平、糖化血红蛋白(HbA1c)水平和体重都有显著的下降。辉瑞已经启动2期临床试验,探索danuglipron治疗糖尿病患者时的效果。据悉,danuglipron的口服特征有望为糖尿病和肥胖症患者提供一款差异化的创新疗法。 3、武田(Takeda):注射用TAK-755 适应症:TTP患者的急性治疗和长期预防性治疗 血栓性血小板减少性紫癜(TTP)为一种罕见的微血管血栓-出血综合征。公开资料显示,TAK-755是武田开发的一种ADAMTS13重组蛋白,它能够在ADAMTS13缺失的患者中补偿ADAMTS13的活性,裂解血管性血友病因子(vWF),从而防止血栓的产生。 在1期临床试验中,这一疗法已经表现出良好的安全性,重组蛋白没有激发机体产生针对它的抗体。武田已经开展3期临床试验,使用TAK-755作为预防疗法治疗先天TPP患者。本次在中国,该药获批的临床研究适应症为:先天性ADAMTS13缺乏(cTTP)患者中TTP的急性治疗和长期预防性治疗。 4、葆元医药(AnHeart Therapeutics):AB-106胶囊 适应症:晚期实体瘤 AB-106(taletrectinib)是一款新型、有效、高选择性的下一代ROS1和NTRK双靶点小分子抑制剂,可穿越血脑屏障。该在研药物最初由第一三共(Daiichi Sankyo)开发,葆元医药于2018年12月获得了该药的全球独家开发、生产和商业化权益。2020年7月,韩国NewG Lab Pharma公司通过与葆元医药达成合作,获得了AB-106在韩国市场的临床开发和商业化授权。 AB-106本次获批的临床研究适应症为:健康受试者及晚期实体瘤患者。值得一提的是,AB-106早前已获批两项临床试验默示许可,针对的适应症分别为携带ROS1融合基因的非小细胞肺癌(NSCLC),以及携带NTRK1、NTRK2、NTRK3融合基因的不分瘤种的实体瘤。其中,针对ROS1融合基因NSCLC的研究已于去年7月进入2期临床阶段。 5、微芯生物:西奥罗尼胶囊 适应症:复发难治广泛期小细胞肺癌




目前,微芯生物正在探索西奥罗尼治疗多种适应症的疗效,涉及复发/难治非霍奇金淋巴瘤、铂难治或铂耐药复发卵巢癌、晚期肝细胞癌、复发难治小细胞肺癌等多种癌症。其中,西奥罗尼胶囊单药治疗经过2线系统化疗方案治疗后疾病进展或复发的小细胞肺癌的适应症,已被CDE正式纳入突破性治疗品种。近日,西奥罗尼再次被CDE纳入拟突破性治疗品种,适应症为联合紫杉醇周疗治疗铂难治或铂耐药复发卵巢癌。
6、重庆药友制药:YP01001胶囊
适应症:晚期实体瘤

根据复星医药公告,YP01001是其控股子公司重庆药友制药开发的一款创新型小分子化学药物,拟用于治疗晚期实体瘤。公告指出,目前,中国境内已上市的该新药同类型药品有甲磺酸仑伐替尼胶囊等。仑伐替尼是卫材(Eisai)公司研发的一种多靶点酪氨酸激酶抑制剂,可以阻滞肿瘤细胞内包括VEGFR1-3、FGFR1-4、PDGFRα、KIT、RET在内的一系列靶点。
(智通财经编辑:林喵)