上市即涨超30%,亘喜生物(GRCL.US)初登美股便感受到了来自华尔街的热情。
智通财经APP观察到,1月8日,亘喜生物正式登陆纳斯纳克。上市当天,亘喜生物盘中股价大涨超50%,最终收涨31.89%,收盘价达到每股25.06美元,目前公司市值已达16.4亿美元。
亘喜生物的上市,意味着截至目前,中国CAR-T细胞疗法公司已经有四家上市,包括美股的传奇生物和亘喜生物以及港股的永泰生物和药明巨诺。从市值横向对比来看,亘喜生物的市值已仅次传奇生物,说明美股市场对于该公司价值的认可。当然,这一价值认可建立在公司扎实的业务发展之上。
做解决行业困难的生意
解决小困难能做成小生意,解决大困难能做成大生意,解决超大困难能成就独一无二的生意。这个生意经放诸四海皆真理。与全球多数致力于CAR-T疗法的“技术流”们不同,亘喜生物的研发更聚焦于解决这一赛道的普遍困难。
在全球范围内,CAR-T疗法普遍面临的重大难题包括:治疗实体瘤有效率低,细胞制备速度慢以及自体疗法成本过高。这些问题极大地限制了CAR-T细胞疗法的市场可及性,影响了研发公司的规模化盈利。只要能有效解决以上问题,就能建立极高的技术壁垒。
从这个角度来看,亘喜生物自主开发的研发平台较产品更为“性感”。
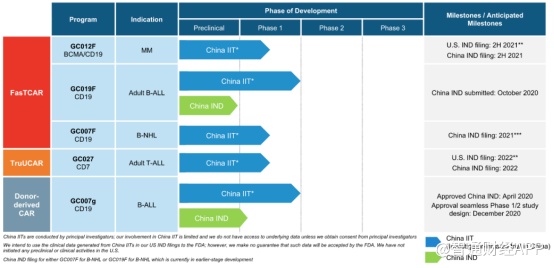
智通财经APP了解到,亘喜生物目前已自主研发出FasTCAR 和 TruUCAR两大技术平台。
FasTCAR平台解决的是细胞制备速度慢的问题。这是一种快速制备CAR-T细胞的方法。众所周知,“激活、转导和扩展”是传统CAR-T细胞制备的三个主要步骤,基于这一技术步骤,制备流程往往需要2周左右的时间。
但在FasTCAR平台技术支持下,可将这三个步骤转化为一个步骤,使得细胞制备能够在24小时左右完成生产,这无疑极大提高了T细胞的生产效率。同时,临床前研究表明,相比传统CAR-T制备方法,FasTCAR平台下生产出的CAR-T细胞显示了更年轻、衰竭更慢、增殖能力更强、更好的组织迁移能力以及更强的清除肿瘤的能力。

在CAR-T疗法中,自体策略存在成本高、等待时间长、T细胞质量参差不齐、治疗实体瘤效果不明显等局限性。然而受限于技术壁垒,全球范围内多数从业公司的开发策略仍以自体疗法为主。
据2020年纽约癌症研究所发表的统计数据,目前大部分在研细胞免疫疗法(667个)仍然属于自体疗法。在这一背景下,同种异体的通用型CAR-T策略被寄以厚望。
亘喜生物另一大核心TruUCAR平台技术,便是致力于解决CAR-T自体疗法的技术局限性。
从全球医学界的研发和临床经验来看,通用CAR-T细胞的制备技术相对复杂,技术壁垒也相对较高。另外,其安全性也一直是研发界关注的焦点,目前通用CAR-T最大的挑战还是在于要克服GvHD和受体对异基因T细胞的排斥反应。
TruUCAR平台技术的解决方案是基于从健康供体获得的淋巴细胞,通过基因改造,以此来避免产生GvHD与排异反应。另外,该技术还能通过遗传修饰防止宿主抗移植物(HvG)反应,并增强TruUCAR T细胞的持久性和增殖。公司可利用该技术开发出源自无需HLA配型的健康供体的T细胞通用型CAR-T产品,有效降低治疗成本,提高CAR-T细胞疗法的市场可及性。
在以上两大核心技术支持下,亘喜生物研发管线中已有5款产品在研,其中3款处于临床试验中。而公司的首个候选产品,用于治疗B细胞急性淋巴细胞白血病(B-ALL)的GC007g,已经进入中国IND新药I期临床试验。这也是国内首个获得临床批件的异体CAR-T产品。
公司核心技术为何具有“革命性”?
与传统的细胞制备技术与自体治疗策略而言,亘喜生物的核心研发平台及其产品无疑是属于“另一条道路”上的产物,但同样也是具有“革命性”的产物。
随着“魏则西事件”的边际影响消退,以及全球行业内细胞疗法研究加速,国内CAR-T疗法在近年逐渐“解禁”,并得以飞速发展,随之而来的商业化问题也浮出水面。
在传统的自体治疗策略下,需要针对每个病人定制化的产品,每个批次的产品需要使用病人自体的T细胞,在应用前需要进行严格的分离筛选,转导激活,灌装质检冷链运输,最后输回病人体内。整个流程耗时2-4周的时间。
抽象来看,细胞的制备其实是根据终端需求订单式生产,病人数量的不稳定导致公司无法对T细胞进行稳定的排产。并且细胞制备背后的固定成本,如生产厂房设备折旧、租金,员工支出以及水电等属于刚性支出,因此不能持续满负荷进行细胞制备,将极大提高公司的成本。
FasTCAR和TruUCAR两大技术之所以是革命性的,在于其从时间和空间两个维度提高了T细胞制备的效率。尤其是通用CAR-T细胞的研发,有望将细胞制备从治疗周期中顺利剥离,将CAR-T细胞疗法从定制化的自体策略中“解放”出来。这也是细胞疗法走向工业化和规模化的基础。扩大市场可及性,意味着细胞制备的排产有望趋于稳定,这将有助于公司实现跨越式的降本提效,形成相对同行的牢不可破的护城河。
当然,以上也仅是细胞治疗企业走向规模化市场的第一步。由于医药行业与普通制造业不同,产品安全性要求保证严格的质量控制和监测,这也是CAR-T生产过程的重中之重。
参考吉利德对于Yescarta的生产质控,主要是从6个方面进行的。生产的原材料试剂、在线监测、在线控制测试、批次发布测试、使用身份链系统实现可追溯性以及制造流程的验证、监控和追溯。这套质量控制体系沿用了前列腺癌DC肿瘤疫苗Provenge的质量管理体系和技术标准,Norvatis和Juno的质量控制体系也沿用了该理念。
然而,细胞治疗作为新兴行业,目前在国内在人才缺乏的背景下,不论培训成本、沟通成本还是管理成本均居高不下,相较于已经步入规模化发展正规的大分子生物药行业而言,还有很长一段路要走。






