本文来源于“医药观澜”微信公众号。
礼来6月9日宣布其胰高血糖素样肽-1受体(GLP-1R)/胃泌素抑制肽受体(GIPR)双重激动剂tirzepatide(LY3298176)的大型心血管结局III期SURPASS-CVOT研究正式完成首例患者给药。
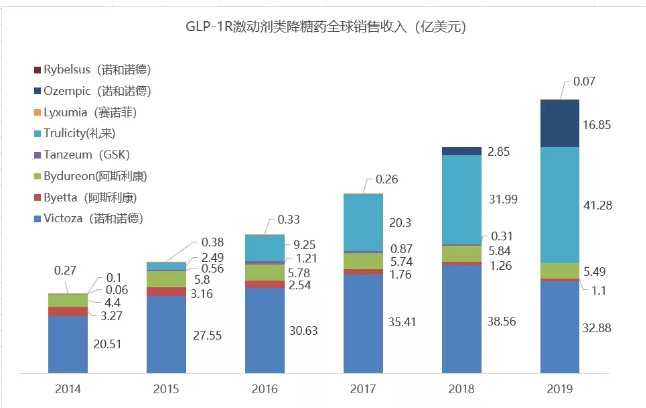
SURPASS-CVOT研究将在全球30个国家入组12500例同时患有2型糖尿病和动脉粥样硬化性心血管疾病(ASCVD)的患者,头对头评估tirzepatide在改善心血管结局方面与长效GLP-1R激动剂Trulicity(度拉糖肽)1.5mg相比是否具有相似(非劣效)和更好(优效)的效果。研究的主要终点定义为3点MACE,即首次出现由心血管死亡、心肌梗死、卒中组成的复合终点的时间。关键次要终点包括全因死亡时间和MACE-3中单个终点的发生时间。Trulicity是礼来当前最畅销的产品,2019年全球销售额达到41.28亿美元,2020Q1同比增长了40%,达到12.29亿美元。SURPASS-CVOT研究拿tirzepatide与自己正处于鼎盛期的王牌产品“头对头”PK多少有一些豪赌的意思,开展这样一个大规模的III期研究对于礼来也是一项巨大的投入。EvaluatePharma预计SURPASS-CVOT研究需要投入高达20亿美元,而评估Trulicity对2型糖尿病患者心血管结局的REWIND研究则需投入大约19亿美元。
SURPASS-CVOT研究的共同负责人、杜克大学医学院内分泌与代谢科主任David A. D'Alessio以及莫纳什大学维多利亚心脏研究所所长Stephen Nicholls博士均表示:“礼来正在进行一次大胆的行动,因为度拉糖肽本身已经证明能够显著降低患者的主要心血管事件风险。”不过从礼来的角度,SURPASS-CVOT研究的完成时间预计需要4年,也就是最晚到2024年,距离Trulicity的专利保护到期还剩3年,这样的赌博值得一试。去年6月的ADA2019年会上,礼来公布的IIb期研究26周结果显示,Tirzepatide在改善2型糖尿病患者的血糖水平和体重方面优于度拉糖肽。
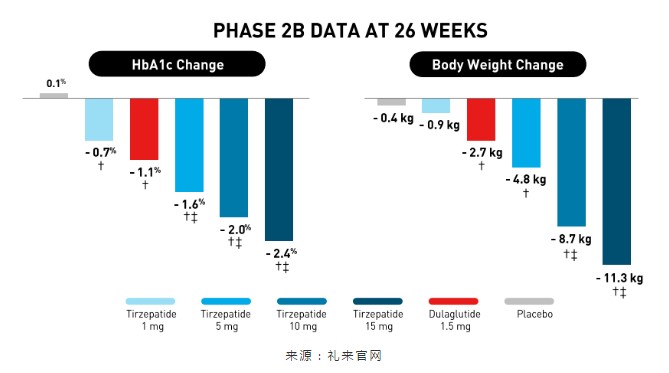
如今,礼来希望借助SUSPESS-CVOT研究证明在同时患有2型糖尿病和心血管疾病的患者中,tirzepatide在改善心血管结局方面是否具有超越同类最佳GLP-1R激动剂的潜力。今年2月,度拉糖肽新适应症获得FDA批准,用于降低伴有心血管疾病或无心血管疾病的2型糖尿病患者的主要心血管事件风险。这也标志着度拉糖肽成为第一个被批准用于一级和二级预防人群降低MACE风险的2型糖尿病药物。改善2型糖尿病患者的心血管结局只是礼来对于tirzepatide开发计划的一部分。礼来目前还在开发tirzepatide针对肥胖的SURMOUNT研究,以及针对非酒精性脂肪性肝炎的SYNERGY研究,所有临床试验开发计划的规模超过了20000人。如若获得阳性结果,tirzepatide的市场潜力上限也将大大提升。
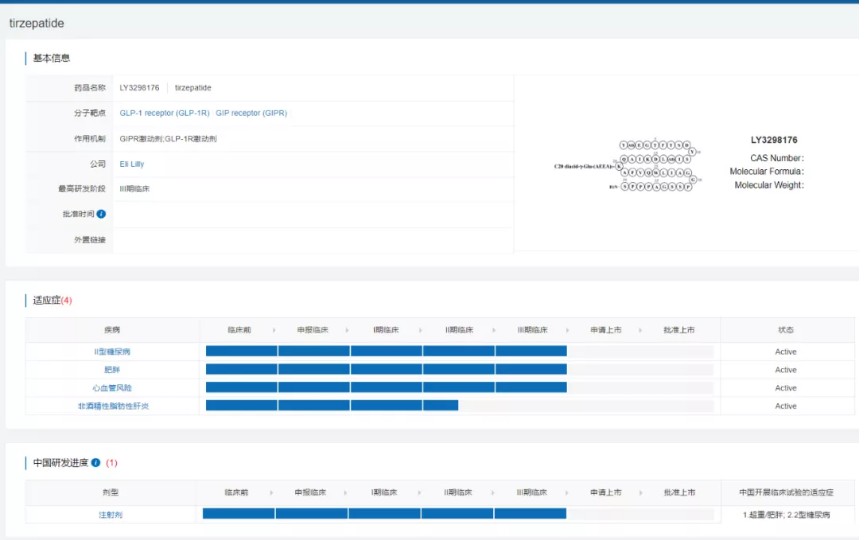
以度拉糖肽、索马鲁肽为代表的GLP-1R激动剂已经将临床治疗糖尿病可以带来的血糖、体重、心血管结局获益提高到了前所未有的高度。口服GLP-1R产品也已经在改善患者治疗依从性方面进一步取得了突破。未来,针对GIPR、GLP-1R的多靶点激动剂或成为糖尿病领域的新药研发热门方向之一。GIP和GLP-1均是能够刺激胰岛素分泌的肠道激素。礼来还有一款针对GLP-1R/GIPR/GCCR的三重激动剂LY3437943目前处于II期临床阶段,诺和诺德和赛诺菲则有同样的三重激动剂NN9423、SAR441255处于I期临床阶段。
(编辑:文文)









