本文来自华西证券。
仿制药集采充分预期,创新价值重构
中国生物制药(01177)目前处于创仿结合的阶段,短期仿制药集采的因素限制了公司业绩的高速增长,但公司通过自主研发与对外合作等多种方式加速丰富创新药物产品线,创新药大幅贡献业绩的拐点很快到来。出色的研发硬实力与专利挑战、立项决策等软实力使得公司在高壁垒仿制药领先于竞争对手,高难度的吸入布地奈德混悬液、干粉吸入剂等呼吸制剂、专利挑战托法替布、奥贝胆酸等重磅首仿,使得公司仿制药业务仍能保持稳定增长。公司的估值有望从龙头制药企业向龙头创新药企业价值重构。
研发与 BD 加速丰富创新管线,销售分线改革
当前国内的创新药环境改变很快,面对审评加速、医保谈判的机遇和进口新药快速进入的挑战,在自主创新方面公司加大研发费用投入、扩增专业研发团队,在外延拓展方面公司 BD 战略部门积极通过 licence-in/out、合营公司、战略投资等方式,加速丰富公司创新药的产品管线,加速向创新转型。在公司产品结构向创新调整的现下,公司 2019 年初推动销售队伍分线改革,精细化管理不同治疗领域销售队伍,更好的发挥协同优势、提高学术推广能力。
盈利预测与评级
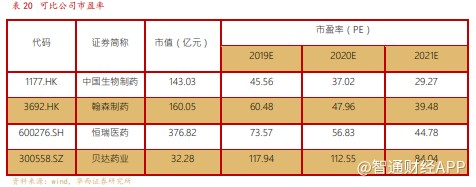
预计公司 2019-2021 年收入 255/302/391 亿元,分别同比增长 22%/18%/30%,归母净利润 33/40/51 亿元,分别同比增长64%/23%/26%(注),当前股价对应 2019-2021 年 PE 分别为 46/37/29 倍。参照恒瑞医药、翰森制药(03692)的估值,给予公司 2020 年 50 倍 PE,目标价 17.94 港元,首次覆盖给予“买入”评级。
注:2018 年,因公司并购北京泰德,对北京泰德的持股比例从 33.6%提高至 57.6%,公司按照北京泰德的最新公允价值,确认原持股北京泰德 33.6%股权的分阶段收购受益 65.99 亿元,从而造成 2018 年公司归母净利润大幅增长,若扣除上述相关因素影响,公司 2018 年归母净利润 28.41 亿元,则我们预计 2019 年归母净利润 32.55 亿元,实际归母净利润同比增长 14.57%。(汇率:1 元=1.121 港元)
风险提示
创新药医保谈判价格大幅下降风险、新药研发及研发进度不及预期风险、仿制药集采未中标或价格大幅下降风险。
1.前言
核心观点:
公司目前处于创仿结合的阶段,通过自主研发与对外合作等多种方式加速丰富创新药物产品线,创新药大幅贡献业绩的拐点很快到来,预计 2022 年创新药占公司收入约 30%。短期仿制药集采的因素限制了公司业绩的高速增长,但公司批量新品种不但可以弥补上集采的影响还能保持仿制药业务稳定增长;并且公司仿制药业务中高端高壁垒仿制药占了很大比重,预计 2022 年收入占比约 20%,该部分仿制药应给予高估值。
由于受仿制药集采未中标影响,我们预测 2020 年公司肝病类药物收入同比下滑 30%(其中我们预测恩替卡韦 2020 年收入同比下滑约 70% ,阿德福韦酯、替诺福韦均下降 40%左右),但受益于抗肿瘤类药品、呼吸系统药品等公司其他优势品类高速增长带动,公司 2020 年整体收入仍可实现 18%增长,净利润同比增长 23%,顺利对冲和度过仿制药集采带来的影响,2021 年开始,公司将轻装上阵,重回快速增长态势,预计收入和净利润分别同比增长 30%和 26%。
报告说明:
公司收入规模、产品线覆盖领域在国内大型制药企业中排名靠前,产品线、核心或重要产品众多,本文受限于篇幅未有全面详尽分析;但研发管线、上市申报产品、新获批产品、一致性评价品种、各治疗领域分类等不同维度都进行了分类表格总结。
创新药、高端仿制药、普通仿制药分类说明:
创新药包括了安罗替尼、PD-1/L1、凝血八因子、生物类似药等产品。
高端仿制药包括吸入布地奈德混悬液、沙美特罗氟替卡松粉吸入剂等呼吸制剂;包括托法替布、奥贝胆酸等专利挑战品种;包括利多卡因凝胶贴膏等剂型创新、适应症创新品种;包括雷替曲塞等 3.1 类独家品种。
2.仿制药集采预期已充分体现,夜尽天晴
公司的仿制药业务在国内大型制药企业中当属最强,出色的研发硬实力与专利挑战、立项决策等软实力使得公司在高壁垒仿制药领先于竞争对手。虽然目前国内在加速推进制药行业的供给侧改革,仿制药集采在日渐常态化,但是公司有批量的大品种仿制药新获批或者即将获批,增量产品对冲了部分不利影响。2015 年开始公司也在加大创新药的研发投入,加速从仿制向创仿结合转型。
第一轮和第二轮集采对公司业绩产生最大影响的主要是肝炎抗病毒的恩替卡韦、替诺福韦、阿德福韦酯等系列产品,对 2020 年的收入影响预计 20 亿元左右。其次镇痛的氟比洛芬酯注射剂、心脑血管的瑞舒伐他汀、厄贝沙坦氢氯噻嗪也有较大影响,对 2020 年收入影响共计约 10 亿元。但是随着布地奈德混悬液、利多卡因凝胶、托法替布、孟鲁司特、福多司坦、西格列汀等新品种放量,能够弥补收入端受集采的影响,维持一定的增长。

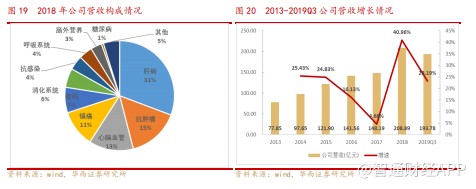
公司的仿制药业务覆盖了多个专科,肝病、抗肿瘤、心脑血管等是公司的重点科室,有 30 多个核心产品销售额过亿,超过 10 亿的有 4 个。在 4+7 集采、4+7 扩面、第二批集采中公司有多个产品纳入集采范围,恩替卡韦、瑞舒伐他汀等品种降幅巨大,对公司业绩产生较大影响。随着集采常态化,公司在集采中更多的新品种将是增量,老品种集采的影响也将逐步消化。随着安罗替尼的高速放量,公司抗肿瘤药物板块收入占比增长明显,随着多个重磅新获批仿制药集采或放量,抗肿瘤创新药的陆续上市,抗肿瘤板块将成为公司最大的专科药业务。
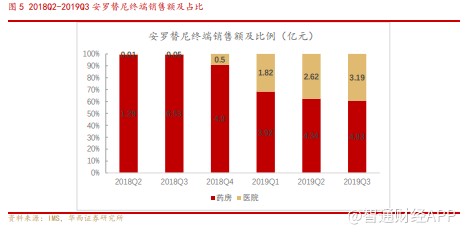
通过下图 1、2 对比可以看出,2019Q3 相比 2018Q3,公司抗肿瘤管线产品收入占比有了显著提升,未来抗肿瘤、呼吸管线将是公司强劲增长的两个领域。

2.1.肝病领域继续巩固,多款早期自主研发新药
肝病是公司最核心的专科领域,主要是保肝降酶和抗肝炎病毒两大类药物。保肝降酶的甘草酸二铵胶囊和注射剂(甘平、甘利欣)、异甘草酸镁注射液(甘美)销售额预计保持稳定。抗肝炎病毒类的恩替卡韦胶囊、恩替卡韦分散片、富马酸替诺福韦二吡呋酯片、阿德福韦酯胶囊由于在第一批集采扩面、第二批集采中未能中标,预计 2020 年销售会有较为明显下降。


在抗肝炎病毒产品线,公司还有多个重磅品种已经在上市申报,预计 2020 年有望获批上市。索磷布韦是吉利德丙肝治愈复方制剂中必不可少的药物,国内丙肝患者每年新发 20 万左右,国产丙肝小分子创新药有北京凯因的 KW-136,歌礼的拉维达韦也即将获批,由于丙肝治愈需要两个小分子联用,国产创新药有望与索磷布韦联合用药。磷丙替诺福韦、恩曲他滨替诺福韦是乙肝治疗最新的药物,公司有望拿下首仿,凭借肝病科室强大销售能力快速放量。
NASH、乙肝的功能性治愈是目前肝病领域创新药物研发的热点,公司在 NASH 领域布局两个创新药物均处于临床早期,海外重磅品种奥贝胆酸公司是国内独家申报企业。TQ-A3334 是一种新型高选择性 TLR7 激动剂,与大型跨国药企强生进行合作正在开展 2 期临床,有望实现乙肝的功能性治愈,想象空间巨大。

2.2.呼吸制剂多高壁垒,率先杀进蓝海
呼吸制剂包括雾化吸入、干粉吸入等多种高端剂型,由于技术壁垒很高,目前原研药在中国处于垄断地位。
公司在 2006 年获批了第一个干粉吸入产品速乐(噻托溴铵),2018 年销售额 6.57 亿元。
公司目前吸入用布地奈德混悬液 2020 年 2 月已首仿获批上市,另一款雾化吸入产品酒石酸阿福特罗雾化吸入用溶液处于上市申请阶段;其中前者 2018 年市场规模 77 亿元。
沙美特罗替卡松粉吸入剂已在上市申报,是一款干粉吸入剂,属于药械一体化产品,技术要求比噻托溴铵吸入剂高,该剂型的成功研发体现了公司在呼吸高端制剂领域强大的技术能力。
目前国内高端呼吸制剂还是蓝海,供给端方面呼吸制剂高技术壁垒限制了仿制的参与者;需求端原研厂家在基层医院还覆盖的较少,而小城市基层医院存在大量慢性支气管炎、肺气肿的患者是目标患者。公司是在呼吸制剂领域仿制开发速度进展最快的公司,近两年公司多个产品的上市将打破原研垄断,在数百亿级的市场中抢占先机。另外公司销售团队是国内药企中规模最大的,在原研未有渗透的县域等基层市场,能够做到全面的覆盖。

2.3.大专科大品种集结,制剂出口探路国际化
在抗感染、心脑血管、糖尿病等领域,公司有批量大专科大品种仿制药新获批上市,其中不乏托法替布、卡泊芬净、利伐沙班等大品种。在仿制药集采的时代,虽然这些大品种都是要集采,给公司带来的利润回报不能与早些年相比。但是对于公司来说,这些都是纯增量品种,批量的产品集采省去推广、营销的时间和费用,也是公司创仿结合转型的合适选择。
公司的氟维司群、替格瑞洛、恩替卡韦等多个仿制药也在欧美等法规国家获批上市,制剂出口探路国际化,为创新药在欧美上市做好准备。另外制剂能够获得欧美法规国家批准,对公司药品质量也是一种肯定,有望享受制剂出口转内销的政策红利。




3.从抗肿瘤领域转型创新,热门靶点布局全面
3.1.抗肿瘤为主的药物创新趋势仍在加强
由于人口老龄化程度加深、生活环境工业污染等因素,癌症已经成为人类健康的第一杀手,癌症的发病率和死亡率越来越高,癌症正成为中国乃至全球首要的死亡原因和一个重要的公共卫生问题。
从 20 世纪末开始,抗肿瘤药物成为全球药物研发最热门领域。以药渡数据库分治疗领域检索,截止 2019 年中,全球在研的创新药仍以抗肿瘤领域最多,处于上市申报、临床 3 期、2 期、1 期的抗肿瘤药物个数占全部领域比例分别为 32%、33%、 41%、48%。临床早期的抗肿瘤药物研发占比更高,则说明了全球抗肿瘤药物为主的新药研发趋势在进一步加速。

抗肿瘤领域是公司创新药物研发的重点投入方向,肿瘤特异性靶点、免疫疗法、抗血管生成等方向公司均有大力布局。在小分子靶向药方面公司自主研发快速追赶,生物类似药多个产品接近商业化,另外公司积极对外合作,投资康方生物、亚盛药业,加速丰富创新药产品管线。


3.2.抗肿瘤仿制药集中获批,雷替曲塞降价 55%进医保
公司在抗肿瘤领域的仿制药也在批量推出,传统化疗药、靶向小分子的仿制产品为公司过渡转型期的业绩稳定打下基础,也为公司在抗肿瘤领域的科室覆盖铺垫。公司凭借强大的研发实力,首仿了阿扎胞苷、雷替曲塞等临床急需的产品,缓解了患者救命药物短缺的情况。




3.2.1.独家品种雷替曲塞谈判进入医保
公司的注射用雷替曲塞(赛维健)于 2009 年获批上市,原研至今尚未在国内上市并且也无其他国产获批。雷替曲塞作为新一代化疗药物,在结直肠癌的一、二线治疗中疗效显著,在 2019 年国家医保谈判中,雷替曲塞首次进入医保限用于氟尿嘧啶类药物不耐受的晚期结直肠癌患者。
雷替曲塞医保谈判价格 669 元每支,较谈判前挂网价格 1500 元降价幅度 55.40%。公司雷替曲塞 2018 年的销售额为 5.12 亿元,结直肠癌患者接受雷替曲塞化疗每次需要使用 3 支药物,一般接受 6 个周期的化疗,按照 1500 元每支药物折算每个患者治疗用药费用 2.7 万,按照销售额折算雷替曲塞覆盖患者约 1.90 万。根据国家癌症统计,2015 年我国结直肠癌患者 37.63 万人,并以年均 2%的增速增长,2020 年预计年新发患者达到 41.55 万人。虽然雷替曲塞进医保降价 55.40%,但是进医保后预计渗透率将会大幅提升,目前仅 5%的渗透率还有很大的覆盖空间,预计雷替曲塞销售额峰值将超 10 亿元。

3.2.2.阿扎胞苷首仿获批
阿扎胞苷是胞嘧啶核苷类似物,是一种具有双重作用机制、目前唯一经临床研究证实能够改善总生存期(OS)的去甲基化药物。其适应症为中高危骨增生异常综合征 (MDS)、慢性粒-单核细胞白血病(CMML)、急性髓系白血病(AML)、骨髓原始细胞为20-30%伴多系发育异常。原研新基的产品于 2017 年 5 月获批进口,2018 年医保谈判价格 1055 元(100mg/支)。
我国骨增生异常综合征每年新发患者约 30 万,高危占比约 10%;急性髓系白血病每年新发患者约 3 万人。阿扎胞苷每四周一个疗程,推荐至少 6 个疗程,每位患者折算治疗费用约 17.7 万-35.4 万。目前阿扎胞苷仿制药仅有公司及四川汇宇两家,在医保逐渐落实到基层的放量推动下,公司阿扎胞苷有望达到 10 亿级别销售额。
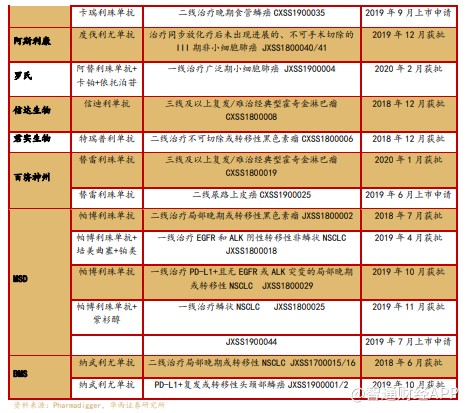
3.3.安罗替尼政策强制进院,PD-1/L1 商业化在即
安罗替尼是一种新型小分子多靶点酪氨酸激酶抑制剂,能有效作用于 VEGFR、 PDGFR、FGFR、c-Kit 等靶点,具有抗肿瘤血管生成和抑制肿瘤生长的双重作用。
安罗替尼于 2018 年 5 月首次获批上市用于三线晚期非小细胞肺癌,软组织肉瘤、三线小细胞肺癌适应症也分别于 2019 年 7 月和 9 月获批。
目前安罗替尼第四个适应症甲状腺髓样癌于 2019 年 12 月上市申报。
另外还有鼻咽癌、食管癌等许多适应症在临床进展中。
与 AK105(PD-1 单抗)、TQB2450(PD-L1 单抗)的联合用药也在快速推进。


安罗替尼 2018 年通过国家谈判进入医保,12mg 规格价格 487 元每片;2019 年再次国家谈判未有降价。由于首次获批是非小细胞肺癌大适应症,且安罗替尼临床数据效果好,2018 年上市首年安罗替尼销售额约有 10 亿元。国家对于 2018 年谈判进入医保的 17 个抗癌药有强制进院的要求,不占药占比,所以安罗替尼在进院方面非常快速。根据米内数据库终端数据放大处理,2019 年第三季度安罗替尼医院终端销售额已达到 40%,预计安罗替尼 2019 年销售额将超过 30 亿元。
2019 年 6 月公司与中山康方成立合资公司,公司以 3.45 亿元出资、中山康方以 AK105(PD-1 单抗)全部权益出资,双方各占 50%权益。目前公司安罗替尼与 AK-105 正在开展多项临床,预计 AK105 与公司自主研发的 TQB2450(PD-L1 单抗)均有望于 20201 年获批上市。虽然公司在 PD-1/L1 产品上市进度稍有落后,但是靠着多方案联用与产品的差异化,AK105、TQB2450 上市后仍有较大市场空间。

3.4.重点布局肺癌,多个靶向药物临床 2 期
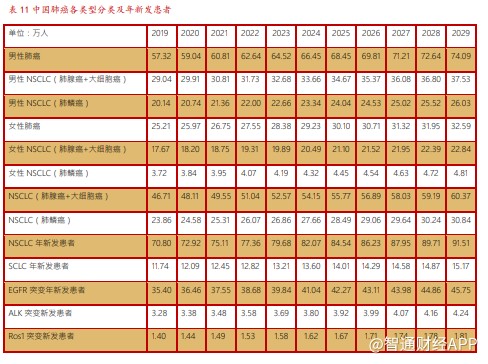
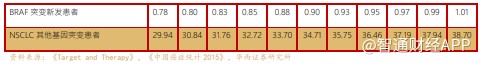
根据国家癌症中心统计的数据,2015 年中国肺癌患者 73.3 万,且以年均 3%的速度增长,其中男性患者 50.93 万人,女性患者 22.4 万人。中国肺癌患者中非小细胞肺癌(NSCLC)占比约 85%,NSCLC 分为三种组织亚型,分别为肺腺癌,鳞状细胞肺癌以及大细胞癌。目前中国的三种亚型分布每年在变化,在所有非小细胞肺癌的亚型中鳞状细胞肺癌的比例在逐年减少,而肺腺癌的比例在逐年上升。根据 2015 年的相关文献显示,中国男性患病者三种亚型的比例为 36.68%(肺腺癌),35.13%(鳞状细胞癌), 13.98%(大细胞癌),而女性的比例为 60.83%(肺腺癌),14.77%(鳞状细胞癌), 9.26%(大细胞癌)。
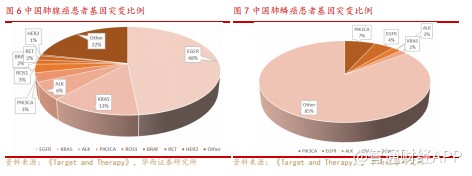
以此估算,2020 年中国非小细胞肺癌(NSCLC)年新发患者 72.92 万人,小细胞肺癌(SCLC)年新发患者 12.09 万人,EGFR 突变的年新发患者 36.46 万人, ALK 突变的新发肺癌患者约 3.38 万人。
3.4.1.三代 EGFR 势在必得,双重保险
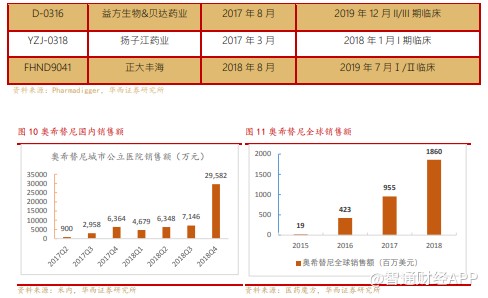
安罗替尼在肺癌治疗中已成为重磅品种,布局更多产品进一步扩大肺癌科室的优势是必然的选择,公司在三代 EGFR 产品开发了两个品种。FHND9041 是正大丰海在研的 EGFR-T790M TKI,目前处于 2 期临床。
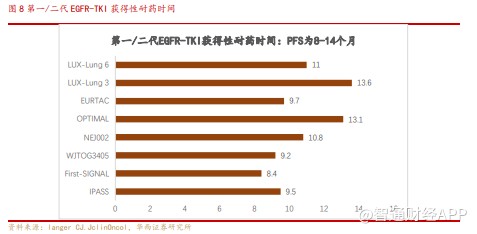
由于疾病进展,几乎所有患者使用第一、二代 EGFR-TKI 靶向药物后最终都会出现耐药,不同患者对靶向药产生耐药的原因不尽相同,但 50%-60%的 EGFR 抑制剂耐药与 T790M 突变有关。根据 langer CJ.JclinOncol 的一篇关于第一、二代 EGFR-TKI 获得性耐药的文献,第一二代 EGFR-TKI 无进展生存期约 8-14 个月。第三代 EGFR-TKI 主要特征就是克服 T790M 突变,最具代表性的就是阿斯利康的奥希替尼。国内 EGFR 突变患者年新增约 36 万,估算 T790M 突变患者每年新增约 20 万人。
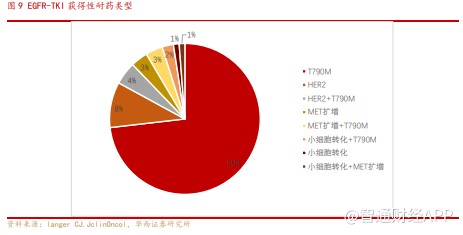
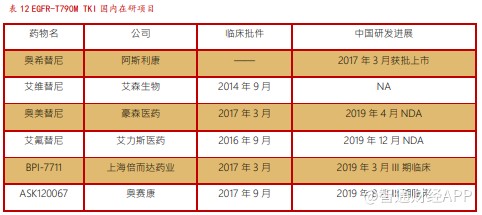
目前国内上市的第三代 EGFR-TKI 仅有阿斯利康的奥希替尼,另有多个产品处于不同的研发状态。奥希替尼于 2017 年 3 月国内获批上市,2018 年 10 月经过国家谈判以 1.53 万元每月的治疗费用进入医保目录,2018 年奥希替尼在中国销售额超过 20 亿元。奥希替尼分别于 2015 年 11 月和 2016 年 2 月获得 FDA 和 EMA 的上市批准,作为 T790M 耐药突变 NSCLC 患者的二线疗法,奥希替尼目前已经在包括美、欧、日、中在内的超过 80 个国家获批。2017 年 9 月,NCCN 指南推荐奥希替尼用于一线治疗局部晚期或转移性 EGFR 突变阳性 NSCLC 患者,作为一线疗法自 2018 年 4 月以来已经在超过 60 个国家获批。
3.4.2.ALK 与 Ros1 单独布局立项,患者少但用药周期长
公司在肺癌领域还单独立项布局了 TQ-B3139(ALK 抑制剂)、TQ-B3101(Ros1 抑制剂)两个创新药,做到了在肺癌领域基本实现了全面覆盖。目前这两个创新药均处于临床 2 期研究,有望以 2 期临床数据有条件上市申请。
ALK 和 ROS1 突变频率在肺癌中不高,但是患者生存周期长,其市场空间也较为可观, 2020 年国内 ALK、Ros1 突变的患者分别约 3.38 万人、1.44 万人。ROS1 与 ALK 存在高度的氨基酸同源性,且患者人群特点也相似,所以目前还未有 Ros1 特异性靶向药物的情况下患者多是使用 ALK 类抑制剂为主,包括克唑替尼、劳拉替尼等。

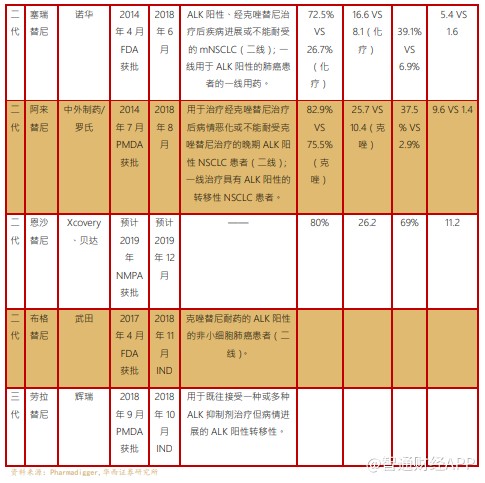
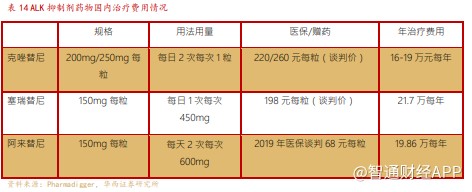
克唑替尼、塞瑞替尼均于 2018 年 10 月国家谈判进入医保,降价后年费用分别为 16- 19 万/21.7 万。阿来替尼在国内刚上市时有“第一年 5+8,第二年 4+9 的赠药政策”,年费用大约 23 万,2019 年国家谈判进入后的年费用 19.86 万。
公司的 TQ-B3139、TQ-B3101 均最快有望年内有条件申报上市,考虑到目前国内已有多款 ALK 抑制剂获批上市,TQ-B3139、TQ-B3101 两个产品定价分别预计 15 万、20 万年治疗费用,销售峰值预计在 5-10 亿左右。
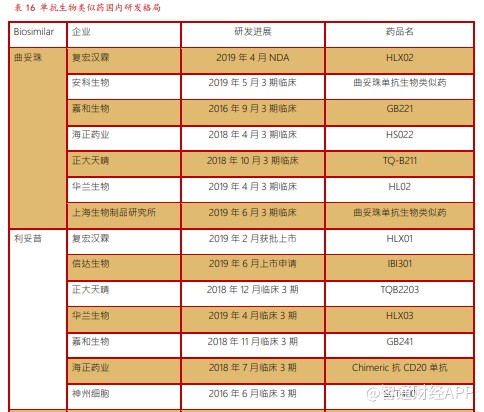
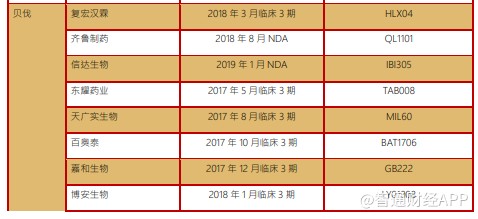
3.5.四个单抗生物类似药有望年内上市申请
2015-2020 年是全球单抗类生物类似药发展的黄金时期,大量原研的单抗药物专利到期,为生物类似药提供了市场竞争的机会。作为世界上人口最多的国家,我国患者基数大,生物类似药市场空间巨大,并且单抗类药物在我国药品市场占比还较小,虽然众多企业跑进该赛道,但生物类似药对大型制药企业仍是不错的选择。
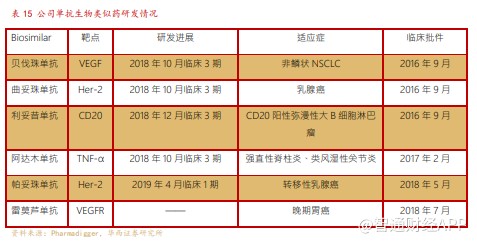
公司目前有曲妥珠、利妥昔、贝伐、阿达木四款生物类似药均已进入 3 期临床,且均有望于年内上市申报。我国法规可以允许生物类似药适应症外推,所以生物类似药产品上市后有望快速放量,抢夺原研产品份额。
4.研发与 BD 加速投入,销售分线改革
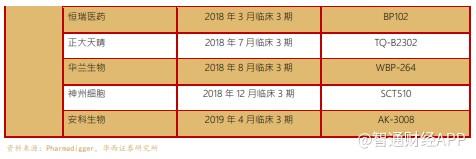
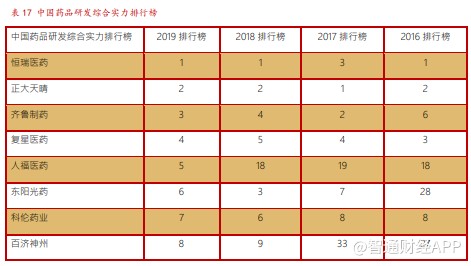
4.1.研发人员大幅扩增,研发投入逐步提高
公司一直以来重视研发的投入,在 2013 年研发投入与营收比达到 8.87%,与 A 股创新药龙头企业恒瑞医药在同一水平,近些年公司药品研发综合实力也一直与恒瑞医药在伯仲之间,在国内大型制药企业或者 Biotech 中排名靠前。
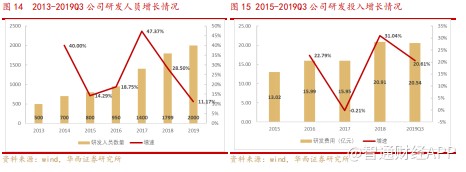
2015 年药审改革从国家层面鼓励创新药发展,公司更加大力投入研发,研发费用持续增长,2019 年前三季度公司研发费用 20.54 亿元,研发投入占比营收达到了 10.63%。从研发投入绝对值看,公司研发投入在中国制药企业中 TOP3;从研发投入占比看,公司研发与营收比与全球大型跨国药企相比还有提升空间,随着公司研发管线推进临床 3 期越来越多、创新药全球多中心临床申报,公司研发投入占比将稳步上升到 15%-20%的水平。
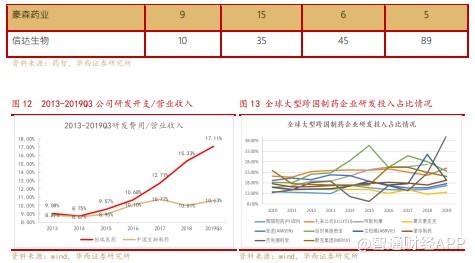
公司研发人员近些年大幅扩张,从 2013 年的 500 人到目前超过 2000 人。其中硕士学历以上的研发人员占比超过 59%,博士学历研发人员比例约 5%。公司的生物大分子研发团队人员超过 240 人,硕士以上的比例超过 80%,相比不差于国内知名生物药 Biotech(复宏汉霖截止 2019 年 3 月研发人员 239 人,君实生物截止 2018 年 4 月 112 人)。
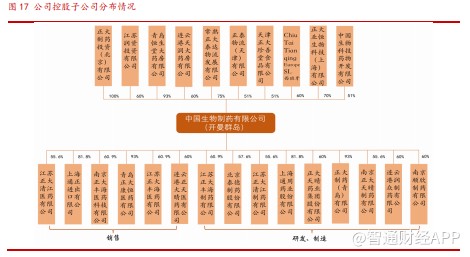
公司共有企业技术中心 5 家,国家级正大天晴技术中心、江苏省级的南京天晴&正大丰海、山东省级正大青岛、北京市级泰德制药。公司共有药品生产、研发控股子公司 9 家,占地 138 万平方米。
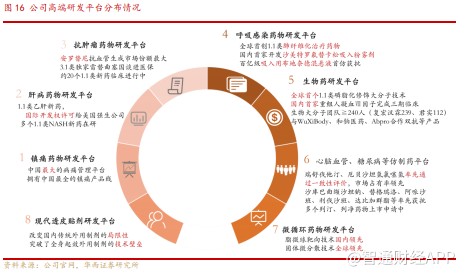
公司以研究院为依托,打造了多个高端研发平台。其中生物药研发平台近几年投入巨大,在研发人员上与国内排名前列的生物药 Biotech 企业相当,并且公司积极的通过委托研发、战略合作、专利授权引进等多种方式与药明康德、和铂医药、Abpro 等国内外技术顶级的研发机构合作。
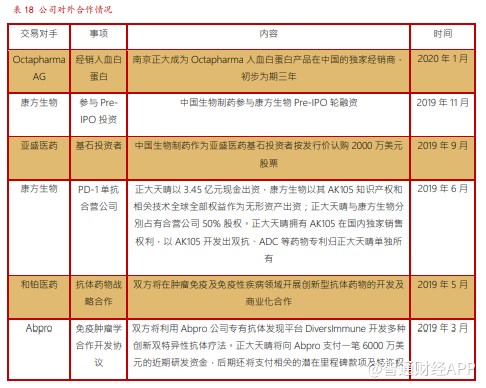
4.2.花钱买时间,BD 部门 Deal 频繁
自主研发大力投入的同时,公司 BD 部门的 Deal 也越来越多。当前国内的创新药环境改变很快,创新药全球竞争者的快速加入(加入 ICH 接受境外临床数据)使得国内 fast-follow 变得更难,而国家医保谈判对同类药物分类谈判使得 me-too/worse 药物医保价格大幅下降。在国内众多企业纷纷转型创新,热门靶点竞争越来越激烈的情况下,通过 licence-in 的方式获得海外产品,“花钱买时间”对于公司这样拥有大把现金流的是个很好的选择。
安罗替尼是公司早期通过 licence-in 的方式获得的一个重磅品种,在抗血管生成小分子药物中市场份额第一,2019 年预计销售额超过 30 亿元。随着全球抗肿瘤药物研发投入越来越多的趋势,公司在抗肿瘤领域与康方生物成立合营公司获得差异化的 PD-1 单抗药物 AK105。另外公司还参与了康方生物 Pre-IPO 轮、亚盛医药上市基石投资者,后续或将有更多的战略合作。

4.3.产品结构改变,销售分线改革精细化管理
公司销售团队在国内制药企业中规模最大,2018 年超过 12000 人的专业学术销售团队与恒瑞医药相当。公司销售网络遍布全国,覆盖全国 90%二级以上医院,产品可下沉渗透到县区级、社区医院。
不同于恒瑞的抗肿瘤、造影、麻醉管线,公司产品管线分布于肝病、抗肿瘤、心脑血管、骨科、消化内分泌、感抗等众多领域,不仅较为分散而且竞争激烈,销售人员的业务能力在激烈市场竞争中充分验证。2018 年公司在肝病用药领域市场占有率达到 25%,术后镇痛领域用药市场占有率超过 66%。
随着公司销售收入整体快速增长、产品线及产品越来越多、产品结构中创新药逐渐增多,公司 2019 年开始进行销售分线改革,将销售人员根据产品科室、适应症分划到不同管线。公司对销售人员管理更加精细化,创新药需要专业的学术推广团队有单独分线的需要,而部分老品种或将受益于分线改革而加速放量。
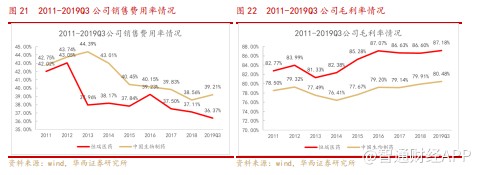
公司销售费用率近几年下降明显,从 2013 年的 44.39%下降到 2018 年的 38.56%。参照恒瑞医药,随着阿帕替尼、吡咯替尼等创新药上市后,恒瑞销售费用率逐年降低。公司销售费用率比恒瑞医药高,主要是目前公司仿制药销售占比高所致。从毛利率的情况可以看出,恒瑞 2014 年阿帕替尼上市后毛利率提升接近 5 个百分点,而公司毛利率基本稳定在 80%左右。
随着安罗替尼高速放量,众多创新药获批在即,接下来公司销售费用率也将逐渐降低。一方面,创新药单价高,销售费用占比相对较低,所以创新药销售收入的占比不断提高,销售费用率将逐渐降低;另一方面,随着仿制药集采常态化,仿制药销售费用被挤掉,也将降低公司的销售费用率。
5.盈利预测及投资建议
5.1.盈利预测
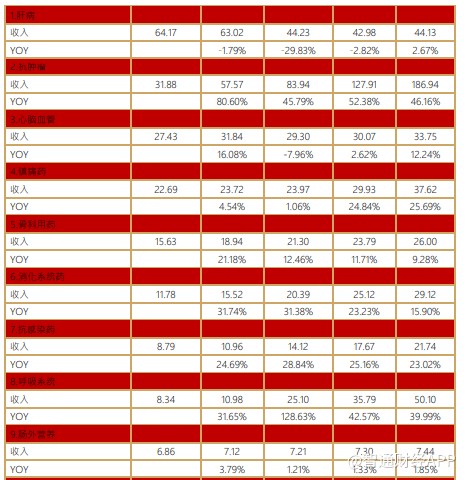
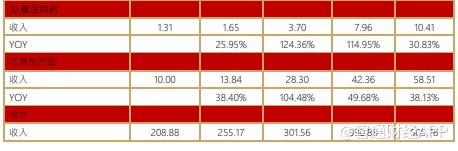
肝病用药受集采影响,2019-2021 年预计收入逐渐下降。润众(恩替卡韦分散片)预计 2020 年收入下降 70%,天丁片(马来酸恩替卡韦片)、甘泽(恩替卡韦胶囊)、名正(阿德福韦酯片)、晴众(替诺福韦)预计逐年缓速下降。
抗肿瘤用药新产品增量巨大,并且老产品快速放量,预计 2019-2021 年高速增长。安罗替尼预计 2021 年将超过 50 亿,雷替曲塞谈判进入医保后预计有 30%的稳定增长,新获批硼替佐米、来那度胺、阿扎胞苷等快速放量。公司肿瘤线产品老产品基数低,即使如阿比特龙集采对公司也是纯增量,预计 2019 年肿瘤线收入增速将达 80%,2020 与 2021 年得益于多款生物类似药、PD-1 产品上市,有望达到 50%左右增速。
呼吸系统用药是公司仿制药增长的新动力,由于呼吸科制剂技术高端壁垒高,国内呼吸制剂基本上是外企原研占据,公司吸入用布地奈德混悬液 2020 年 2 月首仿获批,当年即有望达到 10 亿销售额。速乐(噻托溴铵粉吸入剂)上市 10 多年仍保持 20%以上稳定增长,另外有多款干粉吸入剂上市申请中,在进口替代、挖掘基层市场逻辑下,公司呼吸系统用药 2020 年预计实现翻倍式增长。
镇痛、心脑血管用药由于有大品种被集采,预计 2020 年小幅负增长。骨科、消化系统、抗感染、肠外预计稳定增长,糖尿病用药有多款列汀、列净上市申请或已获批,预计高速增长。另外公司造影剂开始放量贡献业绩,托法替布、凝血八因子均是数十亿级别重磅品种。


5.2.投资建议
公司是国内大型制药企业中综合实力最强的企业,公司在药品研发、销售能力均处于顶尖水平。我们认为公司目前处于创仿结合的阶段,自主研发与对外合作等多种方式加速丰富创新药物产品线,创新药大幅贡献业绩的拐点很快到来,预计 2022 年创新药占公司收入约 30%。仿制药集采虽然短期对业绩有较大影响,但大量仿制药增量品种也能弥补部分,并且公司仿制药板块中高端高壁垒仿制药应给予高估值,2022 年预计高端高壁垒仿制药占公司收入约 20%。
预计公司 2019-2021 年收入 255/302/391 亿元,分别同比增长 22%/18%/30%,归母净利润 33/40/51 亿元,分别同比增长-64%/23%/26%(注),当前股价对应 2019-2021 年 PE 分别为 46/37/29 倍。参照恒瑞医药、翰森制药的估值,给予公司 2020 年 50 倍 PE,目标价 17.94 港元,首次覆盖给予“买入”评级。
注:2018 年,因公司并购北京泰德,对北京泰德的持股比例从 33.6%提高至 57.6%,公司按照北京泰德的最新公允价值,确认原持股北京泰德 33.6%股权的分阶段收购受益 65.99 亿元,从而造成 2018 年公司归母净利润大幅增长,若扣除上述相关因素影响,公司 2018 年归母净利润 28.41 亿元,则我们预计 2019 年归母净利润 32.55 亿元,实际归母净利润同比增长 14.57%。(汇率:1 元=1.121 港元)。
6.风险提示
仿制药集采风险:药品带量采购造成仿制药竞争加剧,仿制药价格下降、市场占有率下降,仿制药的业绩不达预期。
药物研发风险:创新药研发具有高风险高收益的特征,并且公司药物创新 metoo/better 与 first-in-class 同步快速推进,first-in-class 创新药物研发失败风险则更高。
创新药国家医保谈判大幅降价的风险:目前国内创新药物每年国家医保谈判、两年一次续约再谈判已成常态,将创新药尽早纳入医保对企业来说可以快速放量,但国家谈判创新药降价幅度过高,可能会影响产品的营收规模。
新药研发进度不及预期:创新药物的研发需要数十年的时间,临床前、临床 1-3 期、上市申请每个阶段均需要不同的开发时间及等待时间,对创新药物的研发进度无法精准预测。
(编辑:郭璇)






