本文来自微信公众号“米内网”。
跨国巨头辉瑞(PFE.US)公布了2019财年业绩,作为该公司成熟产品之一的普瑞巴林由于专利到期,销售额剧烈下滑,2019年仅为33.21亿美元。该产品于2010年进入国内市场后销售逐年攀升。然而,就在近日,齐鲁制药宣布该公司的普瑞巴林胶囊4类仿制上市申请已获批,成为该品种首家过评企业。这下子,辉瑞能顶住国内高端仿制药带来的冲击吗?
辉瑞超重磅品种,销售峰值超$50亿
图1:辉瑞的普瑞巴林全球销售情况(单位:百万美元)
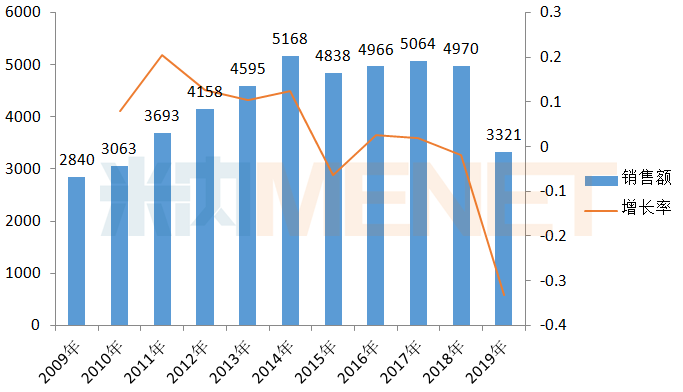
来源:米内网跨国上市公司销售数据库
辉瑞的普瑞巴林商品名为乐瑞卡,2004年获欧盟批准用于管理外周神经病性疼痛及用作部分癫痫发作治疗;同年在美国获批,用于缓解糖尿病性外周神经病相关神经病性疼痛和带状疱疹后神经痛,2005年又获批用于成年癫痫患者部分性发作辅助治疗,2007年再获批用于治疗纤维肌痛,2012年FDA又批准其用于治疗脊髓损伤相关性疼痛。
最近10年,辉瑞的普瑞巴林在全球的销售额均保持在30亿美元以上,其中销售峰值出现在2014年,接近52亿美元,随后有缓慢下滑的迹象,2019年降至33.21亿美元,降幅高达33%。
辉瑞在2019年财报中提到,在美国,乐瑞卡专利原本于2018年12月30日到期,但儿科癫痫项目的开展使其获得了额外6个月的市场独占期。随着专利到期,2019年7月19日,美国FDA同时批准了梯瓦制药(TEVA.US)、雷迪博士实验室等9家制药企业的普瑞巴林仿制药上市,导致全球销售额出现断崖式下滑。
据米内网全球上市药物数据库数据显示,截至2020年2月19日,普瑞巴林的ANDA申请号多达181个,其中中国药企申报占15个。辉瑞在美国市场上受仿制药的冲击与日俱增,中国市场作为辉瑞重要的收入来源之一,情况又如何呢?
辉瑞2010年入华,国产新药2013年获批
图2:辉瑞的普瑞巴林在中国公立医疗机构终端的销售情况(单位:万元)
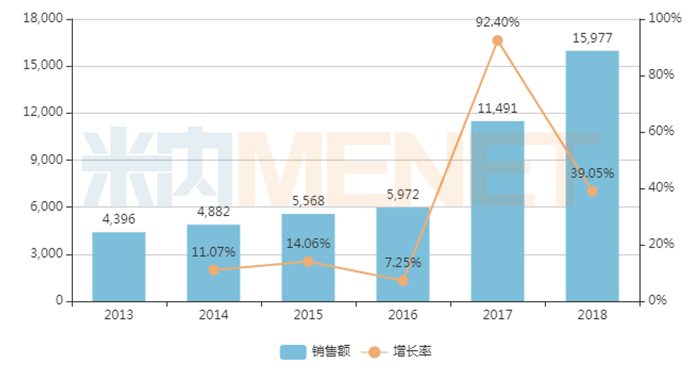
来源:米内网中国公立医疗机构终端竞争格局
辉瑞的普瑞巴林于2010年在国内上市,被批准用于治疗带状疱疹后神经痛,2017年起进入国家医保目录,为乙类,限制使用范围“限带状疱疹患者的神经疼痛二线治疗”,进入医保后该产品的销售额有了飞速的增长。2018年10月15日,辉瑞中国宣布普瑞巴林新增的纤维肌痛适应症上市申请已获国家药监局批准,随后,2019年新版国家医保目录删除了旧版目录中限制使用范围的相关内容。新增适应症叠加医保目录的受限解除效应,预计该产品未来在国内市场的潜力依旧巨大。
图3:国产普瑞巴林的获批情况
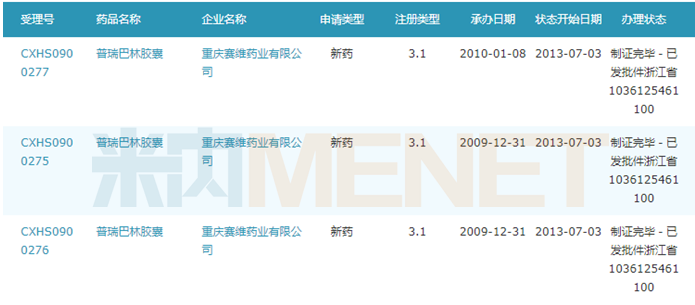
来源:米内网MED中国药品审评数据库2.0
国内药企重庆赛维药业的普瑞巴林胶囊于2013年获批,适应症为成人部分性癫痫发作的添加治疗,注册分类为新药3.1,该企业是目前拥有批文的唯一一家国内药企。产品上市后对原研药的冲击不小,在中国公立医疗机构终端,重庆赛维药业的市场份额从2014年的0.45%上涨至2018年的29.46%,2018年销售额超过6000万元。该产品的一致性评价补充申请于2019年6月获得CDE承办,目前正在审评审批中。
齐鲁釜底抽薪,高端仿制获批成首家过评
据米内网中国药品临床试验公示库资料显示,齐鲁制药的普瑞巴林胶囊在早前的生物等效性试验中对照药物就是辉瑞的乐瑞卡。目前,该产品的4类仿制上市申请已获批,按新分类获批视同通过一致性评价,齐鲁成为了该产品首家过评企业,进入市场后将发起对原研药的强力冲击。
表1:齐鲁制药早前已过评的产品情况
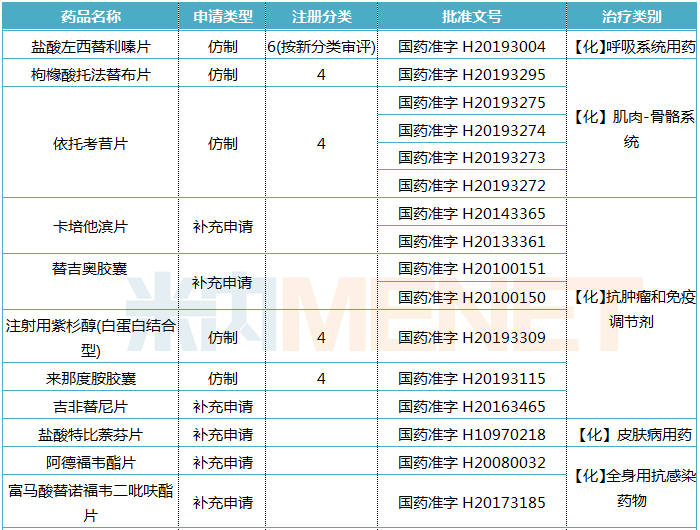

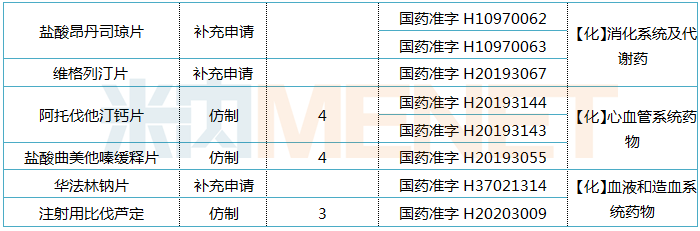
来源:米内网MED中国药品审评数据库2.0
早前,齐鲁制药及子公司已通过一致性评价的产品有24个,其中涉及抗肿瘤和免疫调节剂有5个,神经系统药物有5个。本次普瑞巴林顺利获批视同过评,成为齐鲁制药第六个过评的神经系统药物,也是该企业第25个过评产品,齐鲁“过评大户”名不虚传。
(编辑:李国坚)





