智通财经APP获悉,据医药魔方报道,8月12日消息称,诺华制药(NVS.US)计划2023年之前在中国提交50个新药申请,主要是诺华预计中国的药品审批速度正在加快,可能会使中国超越欧洲成为诺华的第2大市场。据悉,中国的医药市场正在经历一场洗牌,新药的审批速度加快,同时政府部门采取4+7带量采购、GPO等形式限制药价,使一些低价药抢占了跨国企业在中国地区的销售市场。
对此,诺华制药全球药物开发负责人John Tsai在接受采访时表示,诺华公司预计2023年之前将在中国提交50项新药申请,包括创新药和过专利期的品牌药。JohnTsai 还表示,中国将成为诺华的第二大市场。过去4年,中国国家药监局增加了工作人员,并在2017年允许使用海外药物试验数据进行申报,使跨国公司能够更快地将专利产品引入中国市场。 数
据服务商IQVIA数据显示,去年中国药品销售规模达1370亿美元,由于美国政府不断加大降价压力,制药商正寻求新的销售增长来源。
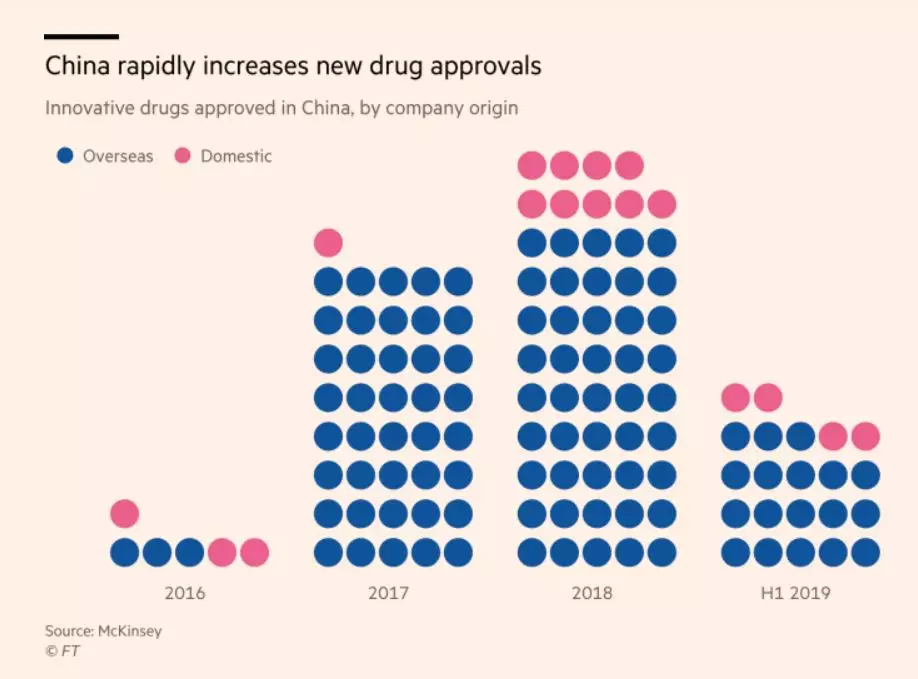
过去,新药在美国获得批准后,需等待长达六年左右的时间才能在中国获批,但如今只需要几个月。在过去2年中,诺华已在中国获批了24种药物,最近一种是7月12日获批用于治疗多发性硬化症的药物Gilenya。2019Q2Gilenya的全球销售额为8.25亿美元,是诺华的第2大核心产品,而它在中国获批仅仅经过3个月。诺华还有其他很多产品也都是借助临床急需药品的“优先审评”制度获批的。
花旗银行数据显示,自2016年以来,诺华通过优先审评途径在中国提交或批准的药品数量超过其他任何外国公司,但其在中国的收入却低于阿斯利康和辉瑞。中国患者如今越来越多地转向国产仿制药,性价比高的国产药更受青睐,且中国的研发能力正在逐渐奋起,在未来的5~10年,可能会迎头赶上。