智通财经APP获悉,2月22日,中国药物临床试验登记与信息公示平台显示,礼来(LLY.US)启动了一项国际多中心3期临床试验(含中国),以评估remternetug皮下注射治疗早期症状性阿尔茨海默病的安全性和有效性。公开资料显示,remternetug是一种抗体新药,靶向一种名为N3pG的淀粉样蛋白亚型。
根据礼来公司公开资料,remternetug(LY3372993)是一款下一代N3pG淀粉样蛋白抗体,采用灵活的给药方案,包括皮下给药,以满足阿尔茨海默病患者的不同需求。此前,该产品已在1b期临床试验中显示出与淀粉样蛋白降低等级一致的深度斑块清除,并且具有较好的安全性。
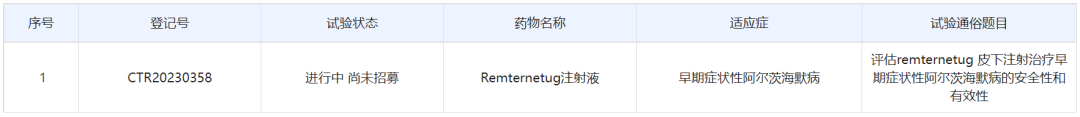
根据中国药物临床试验登记与信息公示平台,此次礼来启动的是一项随机化、双盲、平行分组、国际多中心3期临床试验,主要目的旨在评估remternetug每周一次皮下给药在具有脑淀粉样蛋白和tau蛋白病理的早期症状性阿尔茨海默病受试者中的安全性和有效性。该试验计划在全球入组1300人,中国入组140人,中国主要研究者为首都医科大学宣武医院主任医师贾建平博士。
除了remternetug,礼来在研管线还有多款针对阿尔茨海默病的创新疗法正在不同临床阶段开发中。例如,已在美国申报上市并正在接受监管审查的donanemab,这是一款靶向β淀粉样蛋白的单克隆抗体,并在中国被纳入突破性治疗品种;进入3期临床的靶向Aβ单体的单克隆抗体solanezumab(LY2062430);进入2期临床的O-GlcNAcase抑制剂LY3372689等。






