智通财经APP获悉,据港交所9月8日披露,创胜集团医药有限公司(Transcenta Holding Limited)更新港交所上市聆讯资料,该公司已于6月22日通过港交所聆讯,高盛和中金公司为其联席保荐人。

公司简介:
创胜集团是一家集发现、研究、开发、制造及业务拓展能力为一体的临床阶段生物制药公司。其管理团队及主要业务(包括临床开发、监管准入及业务拓展)位于中国及美国,而发现、研发、工艺开发及生产团队均位于中国。该公司采用全球化策略以最大程度提高运营效率。同时,利用高效的监管审批路径以加快进行在美国的试验用新药(IND)申请及前期临床试验以及推进在中国来自庞大患者人群的巨大医疗需求缺口的适应症的临床试验。公司按可让各试验的临床数据用于进行汇总分析及支持注册(包括中国、美国及欧洲国家)的方式设计试验。此外,多地区临床试验的临床数据使所研究的药物可在其计划的国家及地区进行未来适应症扩展。
业务概况:
截至最后实际可行日期,公司已自主发现及开发9种候选药物中的8种药物,涵盖已验证的、部分验证的及新型生物渠道。MSB2311(一种针对实体瘤的人源化PD-L1单克隆抗体(单抗)候选药物)是其核心产品。基于IMTB技术平台及内部抗体库发现及开发MSB2311。公司就MSB2311采取快速上市策略,并计划开发其用于新适应症。并于2021年1月向国家药监局提交1期结束分析报告,并获准对TMB-H实体瘤患者进行2期试验。除该核心产品外,该公司还有四种主要产品:TST001(一种人源化Claudin 18.2靶向抗体)、TST005(一种人源化PD-L1/TGF-β双重功能抗体融合蛋白)、TST004(一种人源化MASP2靶向抗体)及TST002(一种人源化硬骨素靶向抗体)。MSB2311、TST001、TST005及TST004均由该公司自主开发。
唯一授权引进的候选药物为Blosozumab(TST002)(一种用于治疗骨质疏松的人源化硬骨素单克隆抗体候选药物)。公司于2019年自礼来授权引进Blosozumab(TST002)的大中华区权利。礼来已完成在美国进行的Blosozumab的2期开发。TST002目前在中国处于IND筹备阶段。公司于2021年6月在中国提交IND申请,且申请已于7月6日获国家药监局正式受理。计划凭借礼来的临床数据加快完成于中国的监管程序。此外,公司与礼邦医药组成合资公司以就大中华地区的若干适应症联合开发一种针对肾病自主开发的人源化MASP-2单克隆抗体候选药物TST004。公司保留世界其余地区的权利和在大中华区针对许可适应症以外的适应症开发TST004的权利。
财务概况:
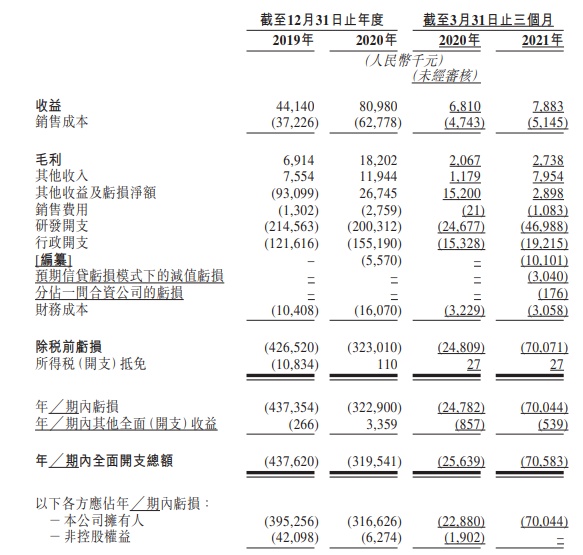
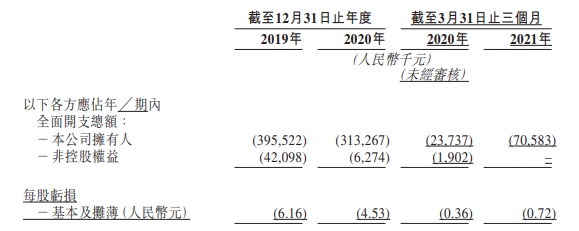
于往绩记录期,公司的绝大部分收益来自根据合约研发生产组织(CDMO)合约向客户(主要为制药及生物科技公司)提供CDMO服务。该公司目前尚无获准可进行商业销售的产品,因此并未产生任何产品销售收益。
于2019年、2020年截至12月31日止及2020年、2021年截至3月31日止三个月,公司的总收益分别为4414万元、8098万元及681万元、788.3万元(人民币、下同)。毛利润分别为691.4万元、1820.2万元及206.7万元、273.8万元。