在抗肿瘤药物过度竞争的时代,审美疲劳也与日俱增,不少企业开始布局专科药物,眼科药物、呼吸系统药物、皮肤科药物、抗病毒药物公司也越来越多的涌现。
成立于2013年的上海爱科百发生物医药技术公司(以下简称爱科百发)在6月29日向港交所递交招股书。
智通财经APP了解到,爱科百发是一家创新的生物制药公司,专注于发现和开发新型疗法,以应对呼吸系统和肺部疾病方面未被满足的医疗需求。公司的候选药物产品组合涵盖整个疾病周期和患者细分,可突出应对一系列目前缺乏有效治疗的急性和慢性呼吸系统和肺部疾病。
招股书显示,爱科百发已开发的产品管线具有九种候选药物,其中包括以Ziresovir(潜在首款治疗相关疾病且接近商业化的药物)为首的RSV药品组合,以及以AK3280(潜在的同类最佳且处于临床阶段的IPF药物)为重点的抗纤维化药品组合。自从罗氏获得Ziresovir分子的许可以来,公司已经迅速推进了Ziresovir的9项临床试验,适用于美国、中国、欧洲和澳大利亚等主要市场的儿科和成人患者,现已于中国开展III期注册试验。
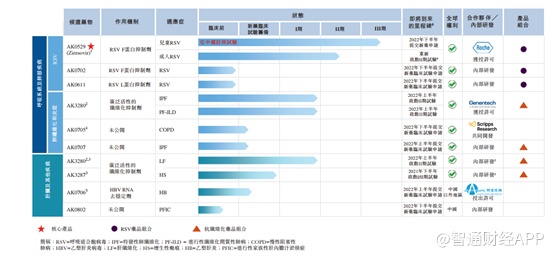
RSV是一种极为普遍且具有传染性的有包膜的RNA病毒,会引起呼吸道疾病,尤其是在易感人群(如儿童、老年人及免疫功能受损者)中。RSV通常于上呼吸道中开始感染,引发的症状易与普通感冒相混淆,因此诊断率相对较低。倘无法得到适当治疗,则RSV病例或会发展为临床表现更严重的下呼吸道感染并且将可能进一步发展为慢性呼吸系统和肺部疾病。
就公司的核心产品Ziresovir来说,该药物是一种靶向F蛋白的新型、潜在用于治疗RSV的首创药物。
RSV感染是引起全球幼儿下呼吸道感染的首要诱因,2岁以下儿童感染率为90%,全球每年约330万儿童感染并住院。2020年,全球五岁以下儿童RSV严重感 染发病人数达3460万人,中国为300万人。据估计每年全球65岁或以上成人中亦有5.5%感染RSV,原因为他们的免疫系统因老化而逐渐退化。2020年,全球65岁或以上成人严重RSV感染发病人数达490万人,中国为120万人。
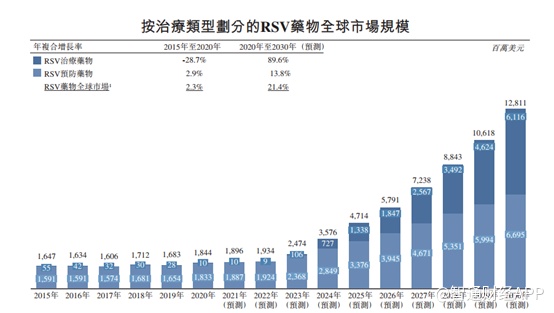
随着老龄化的加速,RSV药物全球市场(包括治疗药物及预防药物)预计将从2020年的18亿美元增至2030年的128亿美元,年复合增长率为21.4%。 RSV治疗药物的全球市场规模历来受到缺乏有效治疗方法的限制。根据灼识咨询报告,在RSV治疗药物的预期上市及其可及性增加的推动下,预计RSV治疗药物全 球市场将大幅增长,到2030年达到61亿美元,自2020年的年复合增长率为89.6%。随着预防效果更好、持续期更长、患者覆盖面更广的新型预防药物在未来几年内进入市场,预计全球RSV预防药物市场将会上升。
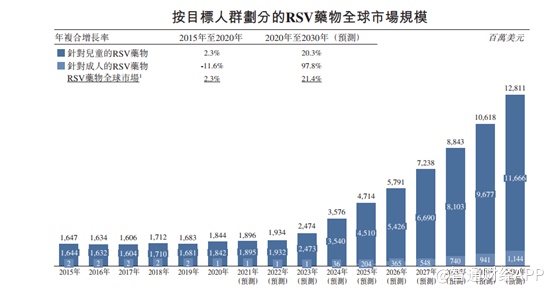
获批准及临床阶段RSV治疗和预防药物主要针对最易患病的儿童,因此根据灼识咨询报告,针对儿童的RSV药物的全球市场预计将以20.3%的年复合增长率由2020年的18亿美元增至2030年的117亿美元,将占全球RSV药物市场的约91.1%。
整个中国RSV药物市场预计将自2020年的520万美元大幅增至2030年的15亿美元,年复合增长率为75.8%,根据灼识咨询报告,其中针对儿童的RSV药物预计约占整个中国RSV药物市场的89.4%。 根据灼识咨询报告,随着潜在疗效更佳的新型RSV抗病毒药物在中国上市,预计到2030年,中国的RSV治疗药物市场将增至11亿美元。由于帕利珠单抗未在中国获批,RSV预防药物中国市场迄今仍处于空白,且预计将于2027年首款RSV预防药物预期在中国上市后兴起。

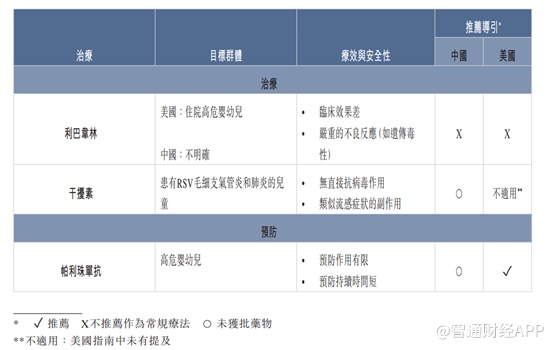
到目前为止,尚无专门针对RSV的有效治疗方法。RSV的标准治疗仅限于支持性护理,例如氧气、鼻塞缓解剂、营养及水分补充以及使用支气管扩张剂、肾上腺素及类固醇。美国和中国的主要临床实践指南并不推荐使用利巴韦林(一种并非专门针对RSV的广谱抗病毒药物),原因是担心其潜在毒性、有限且不可预测的功效以及与雾化给药相关的不便和高成本,一名患者每天可能需花费平均29000美元。
在中国,目前还没有专门批准用于RSV儿童患者的现有 RSV药物。近年来直接抗病毒药物剂作为治疗RSV的新候选药物正在开发中,其主要针对参与病毒复制周期的各种蛋白质, 包括融合蛋白(F蛋白)、核蛋白(N蛋白)及RNA聚合酶(L蛋白)。
干扰素是一种适应症外广谱药物,在中国用于治疗患有RSV毛细支气管炎和肺炎的儿童。帕利珠单抗(一种专门针对RSV的单克隆抗体)是全球唯一获得批准的RSV预防药物,惟仅适用于个别高危婴幼儿,并且在中国未获批准。帕利珠单抗在流感季节需要每月注射一次,且单剂量成本为1000美元至3000美元(取决于患者的重量)。尽管帕利珠单抗预防效果有限、预防持续期短且患者覆盖面窄,其全球年销售额在过去十年内达到16亿美元的峰值。全球并无其他获批准用于预防RSV的预防性抗体药物或疫苗。
截至最后实际可行日期,全球有四种针对RSV的抗病毒化合物处于临床开发阶段,主要为F蛋白和N蛋白靶点。
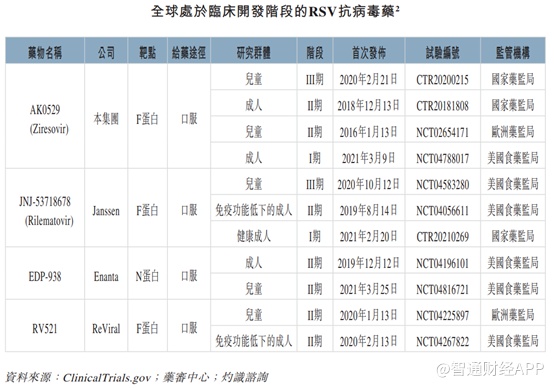
爱科百发引进的Ziresovir是针对儿童这一群体,在2020年2月已经获得国家药监局三期临床试验,具有重大商业化机会。由于有卓越的临床表现及安全性,Ziresovir是首款获得国家药品监督管理局突破性认定的非肿瘤药物,并且将有资格获得加速监管审查,预计将在2022年上半年完成试验。
如果试验良好,公司预计将在2022年下半年向国家药品监督管理局提交新药上市申请,并于2023年在中国开始商业化。
尽管公司尚未有产品商业化,也没有从产品销售中产生任何收入,但凭借着Ziresovir这款产品,爱科百发依旧吸引一众知名投资者,如高瓴资本、启明创投、泰福资本、TPG等赫然在列,并且经过8轮融资,融资后估值高达38.7亿人民币。






