本文来自 微信公众号“DeepTech深科技”,作者: 刘军。
吉利德科学(GILD.US)成为今年制药行业的大明星。
他们先是凭借新冠 “疑似特效药” 瑞德西韦收获了全世界的关注,接着在今年 9 月中旬,吉利德宣布了本年度制药行业最大的一笔收购:210 亿美元收购 Immunomedics(IMMU.US)。这是一家专注于抗体偶联药物(Antibody Drug Conjugate,简称 ADC)研发的美国企业。
这笔巨资收购的背景值得玩味。
豪掷 210 亿美元的背后
吉利德曾经专注于艾滋病和丙肝治疗,但随着专利到期、仿制药竞争,这两大业务无法支撑公司持续增长。从 2017 年开始,公司转型,大举进入癌症治疗领域,一系列的并购投资彰显了吉利德押注癌症治疗业务的决心。
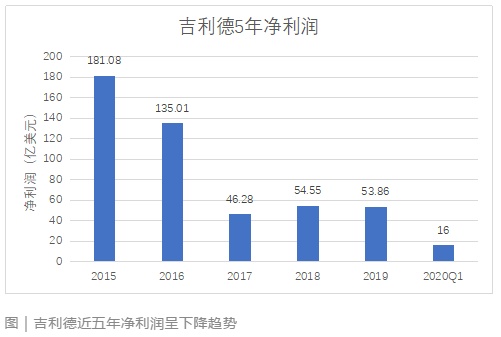
三年,五次出手。这次收购吉利德豪掷 210 亿美元,基本花光了公司持有的全部现金。资料显示,截止 2019 年底,吉利德公司账户现金达 243.5 亿美元。为了顺利完成交易,公司动用了现金账户中的 150 亿,外加债券融资 60 亿。

很明显,在吉利德看来,这次“抓了一条大鱼”。吉利德凭什么看中 Immunomedics?后者手里抓了一手什么样的王牌,值得吉利德做出近乎孤注一掷的如此举动?
Immunomedics 成立于 1982 年,致力于抗体药物和 ADC 的研发。但是在 2020 年之前,它没有一款新药上市。直到 2020 年 4 月,公司的沙伊图珠单抗(Sacituzumab govitecan,药名为 Trodelvy)获美国食品药品监督管理局(FDA)加速批准,成为全球首个治疗三阴性乳腺癌的抗体偶联药物。不止于此,Trodelvy 也成为首个针对 Trop-2 靶点的靶向药物。
Immunomedics 是 38 年磨一剑,吉利德更是 210 亿美元掷一注。
对此,药明生物执行董事、执行副总裁兼首席技术官周伟昌博士告诉 DeepTech:“已有临床数据显示,Trop-2 是一个很重要的靶点,除了在三阴性乳腺癌,该靶点在多种实体瘤中均有表达。”
这意味着吉利德看似买了一款药,其实未来可能治疗多种癌症。公开资料显示,Trop-2 在各种人类上皮性肿瘤中表达更高,包括乳腺癌、肺癌、胃癌、结肠直肠癌、胰腺癌、宫颈癌和卵巢癌等,或者这才是吉利德愿意出高价的真正原因。
Trodelvy 作为 Immunomedics 的拳头产品,三期临床疗效显著,以无进展生存期(PFS)指标来看,接受该药物治疗的患者 PFS 中位数为 5.6 个月;与之对比,接受化疗的患者为 1.7 个月。
PFS 指的是“患者在治疗某种疾病或治疗后的时间内,患者与疾病共存,但是疾病不会恶化的持续时间”,该指标用以判断药物治疗肿瘤方面的疗效。PFS 从 1.7 个月增加到 5.6 个月,差距已经足够显著。
当前,全球已经有 9 款 ADC 药物上市,其中 6 款是近两年上市的。根据美国市场调研公司 Grand View Research 预测,到 2025 年,全球 ADC 市场规模将达到 99.3 亿美元,未来 5 年将保持 25.9% 的年复合增速。
浙江新码生物医药公司(下称新码生物)董事长梁学军对 DeepTech 表示,ADC 的一大优势就是可以批量、工业化生产,从而降低了治疗费用,“未来使用 ADC 治疗癌症,每年费用可以控制在 20 万人民币左右。”这和当前火热的另一种癌症治疗方法 CAR-T 疗法相比有明显优势:CAR-T 疗法由于需要定制,价格昂贵,查询公开资料得知,全球第一款上市的 CAR-T 药物、来自诺华公司的 Kymriah,一次性治疗费用需 47.5 万美元。
ADC 由三部分组成,单克隆抗体、毒素分子和用于连接它们的连接子(Linker)。
当 ADC 注入人体后,其杀死癌细胞的过程可分为 3 步。
第一步,利用单克隆抗体靶向性,找到癌细胞,ADC 与靶癌细胞结合。
第二步,癌细胞通过内吞作用,把 ADC“吃到肚子里”。
第三部,ADC 分子被癌细胞溶酶体溶解,毒素分子释放,癌细胞被杀死。
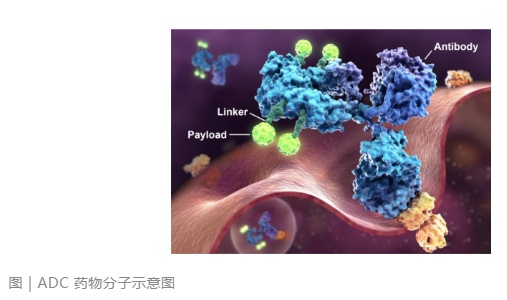
ADC 药物有点像是拼凑起来的变形金刚。毒素分子来源于癌症化学疗法,而单克隆抗体要追溯到上个世纪 70 年代。ADC 的诞生是医学多种子领域共同进步的结果。
用 100 年寻找“神奇子弹”
哈佛大学丹纳 - 法伯癌症研究所(Dana-Farber Cancer Institute)是全球知名的癌症研究中心之一,该机构的名字是为了纪念现代化疗之父——西德尼 · 法伯(Sidney Farber)。
1947 年底,受叶酸促进癌细胞增殖的启发,法伯反其道行之,通过给白血病患者注射叶酸拮抗剂(抑制叶酸活性),16 名患者中有 10 名病症得到了暂时缓解。此后,经过一系列实验,法伯开创了癌症的现代化学疗法。
所谓癌症化疗,就是用能杀死癌细胞的化学毒素来治疗癌症。在化疗诞生之初,医学还没有揭示癌症的深层次成因,肿瘤医生和化学家只能通过大量实验,去寻找那些能够杀死癌细胞的化学物质。从 1954 到 1964 年,美国癌症化学疗法国民服务中心(CCCNSC)测试了 8.27 万种化学合成试剂、11.5 万种发酵产品和 1.72 万种植物衍生物,每年对 100 万只小鼠开展各种化学实验,就是为了找到一种理想的杀死癌细胞的药物。
但每一种化疗药物,都逃脱不了 “杀敌一千,自损八百” 的魔咒。细胞毒素在杀死癌细胞的同时,也会杀死健康细胞和人体免疫系统,化疗到最后往往成为了 “人和癌症谁先死亡” 的竞赛。
上世纪 80 年代,正是癌症化学疗法大发展时期。化疗师们尝试各种化学毒素的排列组合,越来越多的药物进入临床试验,越来越强的副作用随之而来。时任国家癌症咨询委员会成员的罗丝 · 库什纳写道:“当医生说副作用是可忍受或可接受的时候,他们其实是在谈论可危及生命的东西。就算你呕吐到眼睛血管爆裂…… 他们也认为不值一提。”
肿瘤医生面对病人更是两难抉择:一边是没有把握的新药物组合(副作用),一边是无可逃避的死亡。寻找只会杀死癌细胞,而不会损伤健康细胞的化学药物,仿佛是一个幻想。
但科学家的这种努力从未停止过。
早在 1900 年,德国诺贝尔奖获得者保罗 • 埃利希 (Paul Ehrlich) 提出了 “神奇子弹” 的概念:让有毒的分子注入人体,攻击癌症细胞而不损伤周围的健康细胞。“神奇子弹”的提出要早于现代化学疗法的诞生。
化疗药物是一种子弹,为这颗子弹嵌入“神奇”,则要追溯到 1975 年。
这一年,乔治 · 科勒(Georges Kohler)等人设计了杂交瘤技术,产生了一种特殊的抗体。这种抗体由单一 B 细胞克隆产生,高度均一,且只针对某一种特定的抗原起作用,称为单克隆抗体。
单克隆抗体由于具有靶向性,很快被应用于癌症治疗。单克隆抗体治疗某些特定癌症的机理是,通过与癌细胞特异性结合,减缓、阻断其增殖,或者介导免疫细胞杀死癌细胞。
另一种技术路线则是,对单克隆抗体进行修饰,让它携带细胞毒素,精准找到癌细胞,释放毒素杀死后者。这就是抗体偶联药物(ADC),也是保罗 • 埃利希设想的“神奇子弹”。
2000 年,由辉瑞(PFE.US) / 惠氏研发的 ADC 药物 Mylotarg 获得美国 FDA 批准上市,虽然迟到了 100 年,后又因安全问题退市,但是首个 ADC 药物的诞生给癌症治疗带来了新曙光。
简单地理解,癌症 ADC 疗法,就是靶向化疗。
创新性靶点:新希望、高风险、高收益
周伟昌说,和传统单克隆抗体药物相比,ADC 的研发和生产要复杂许多倍。ADC 药物由单克隆抗体、毒素分子和连接子组成,将这三部分组合起来并不容易。单克隆抗体属于生物药,毒素属于小分子药物。想要做 ADC,企业必须能同时生产抗体、毒素和连接子,也要有足够的资金实力。早在 1997 年,全球第一个单克隆抗体利妥昔单抗(Rituximab)就上市了。而第一个 ADC 药物(Mylotarg)在 2000 年才上市,并且因为安全性问题在 2010 年退市,2017 年再次上市。
ADC 研发难点在于,要将靶向(单克隆抗体)和化疗(细胞毒素)用连接子稳定连接起来。周伟昌介绍,一个好的连接子,要满足两个条件。
第一个条件是:它既要稳定,又要不稳定,找到两者之间的平衡点需要开展大量研究。稳定是说连接子在血液中无法被分解,否则连接子提前断裂,毒素在到达目的地之前被释放,就会杀死健康细胞;而当 ADC 进入癌细胞之后,连接子要能正常分解,从而释放毒素杀死癌细胞。
第二个条件,是尽量保证每个单克隆抗体连接的毒素分子一样多。这一点恰恰是非常难做到的事,涉及到分子层面的操控。一般来说,毒素分子是通过双硫键连接到抗体身上,如果每个抗体连接的毒素分子数量不一致,则很可能同一批药物,病人有时候产生较大的副作用(毒素溢出癌细胞),有时候没有效果(毒素太少)。
在这一点上,新码生物采用了不同于双硫键的偶联技术。梁学军介绍,他们使用非天然氨基酸连接抗体,再将毒素分子连接到非天然氨基酸上,这样做的好处是毒素分子连接稳定,数量可以精确控制。
去年底,新码生物公布了其 ADC 在研产品 ARX788 的一期临床数据。数据显示,ARX788 在晚期 HER2 阳性乳腺癌患者中,表现出很高的响应率,而且同时几乎没有产生类似其他 ADC 类产品的血液毒性。梁学军认为,这得益于新型偶联方式的稳定性。
当前,国内进展较快的 ADC 药物是百奥泰的 BAT8001,已进入临床三期。资料显示,BAT8001 使用了自主研发的连接子,毒素分子则采用美登素(maytansine)。作为国内首个进入临床三期的 ADC 药物,BAT8001 预计 2021 年完成临床工作并申报中国 NDA(新药申请)。
根据数据统计,截止到 2020 年 9 月,如果计算国外药企的 ADC 产品在中国进行临床试验的情况,全球进入临床阶段的 ADC 药物,美国有 66 个,中国有 14 个。其中,已经上市的 ADC 药物,美国有 9 个,中国仅有 2 个(罗氏集团的 Kadcyla 于 2020 年 1 月获批和武田制药的注射用维布妥昔单抗,于 2020 年 5 月获批)。

从上图中可以看到,当前国内 ADC 产品均以 HER2 为靶点研发。HER2 是抗体药物研发中最经典的靶点之一。作为老靶点,针对它的单克隆抗体研发技术已经成熟,技术也经过多次迭代,开发难度较低。国内企业选择以 HER2 为靶点发开 ADC 药物,主要考量是风险 - 收益权衡。
而这次被吉利德看中的 Trodelvy,是第一款针对 Trop-2 为靶点的靶向药物——它被称为创新性靶点(Innovative Target)。
为什么 Immunomedics 可以卖到 210 亿美元?这与靶点的价值直接相关。
国外专门研究药物研发的机构 Tufts Center 曾经给出了一组数据,展示了开发一款新药的成本到底有多高。数据显示,药物开发周期从临床前靶点筛选到最终上市,平均至少 13.5 年(不包括靶点确认阶段),其中临床前要 5.5 年,临床开发要 8 年。反映到资本成本上,开发一个新药,平均耗资 13.95 亿美元,如果将资本时间成本和机会成本折算进去,这个数字为 25.58 亿美元。
但国内药企开发新药成本却要低得多,平均仅在 3 亿人民币左右。举例说明,恒瑞的吡咯替尼研发成本是 5.2 亿元,PD-1(报产)是 1.55 亿元,阿利沙坦酯也不到 3 亿元。
为何国内外新药研发成本差距如此之大?原因就在于两个字:风险。国内企业大都做的是 me-too 类药物,失败风险较低。从 ADC 药物均以 HER2 靶点开发可以看出这一点。
跟进式开发并不等于只有好处(低投入),同质化竞争会带来新的问题:后开发者的收益难以保证。
这从侧面说明了为何一个 Trop-2 靶点就能撑起 Immunomedics 公司的 210 亿美元估值。作为第一个上市的 Trop-2 靶点靶向药物,第一个吃螃蟹的人,公司承担的风险必然要折算到研发成本里;一旦成功,其收益也远非跟进式研发成果可比。
高风险,高收益,这是再简单不过的常识;更重要的是,Trodelvy 三期临床给出的初步数据乐观,已经足以折服吉利德。
仅仅是最近两年,FDA 已经批准上市了 5 个 ADC 药物。有观察者认为,这预示着生物制药公司从过去十年的临床试验经验中摸索出了解决 ADC 复杂设计难题的策略;吉利德的重磅交易更是把 ADC 的研发热度推向了高潮,这一重磅交易势必激励国内外更多生物公司进军 ADC 战场,靶向化疗大门已经开启。
(编辑:赵锦彬)






