本文源自“医药观澜”微信公众号。
近日,罗氏(RHHBY.US)与Vividion Therapeutics达成一项数十亿美元的全球独家许可协议,以利用后者的蛋白质组学筛选平台和专有的小分子数据库,开发创新的蛋白降解疗法。这项合作再次引起人们对蛋白降解疗法这一新型治疗方法的关注。
事实上,罗氏并不是唯一一家通过合作布局这一领域的公司。公开信息显示,近几年,葛兰素史克(GSK.US)、默沙东(MSD.US)、辉瑞(PFE.US)、拜耳(BAYRY.US)等多家全球性药企,已就蛋白降解疗法与不同的公司达成了十几项合作。而资本市场,也对这一领域青睐有加,前不久,专注于这一创新疗法的两家公司Kymera和Nurix均完成了超1亿美元的融资。
那么,蛋白降解疗法究竟是什么?它有什么独特之处?全球性药企和资本为何如此看好它?
细胞里的“垃圾处理站”
蛋白降解疗法的原理是基于细胞里的“垃圾处理站”——泛素-蛋白酶体系统(ubiquitin-proteasome system,
UPS)。泛素-蛋白酶体系统于上世纪70年代末、80年代初被科学家发现,它是细胞内蛋白质降解的主要途径,参与了约80%以上的蛋白质降解。
泛素-蛋白酶体系统由泛素、泛素活化酶(E1)、泛素结合酶(E2)、泛素连接酶(E3)、蛋白酶体及其底物(蛋白质)构成。在泛素-蛋白酶体系统中,细胞会给需要降解掉的蛋白质添加上一些泛素分子,这就好像是给“垃圾”打上了“可回收”的标记。然后,这些被泛素标记的蛋白质会被送到细胞内的蛋白酶体处。后者就像是垃圾处理中心,能把蛋白质分解成短肽和氨基酸,供细胞合成其他蛋白质使用。2004年,诺贝尔化学奖授予给了发现这一机制的三名科学家,以表彰他们所做的贡献。
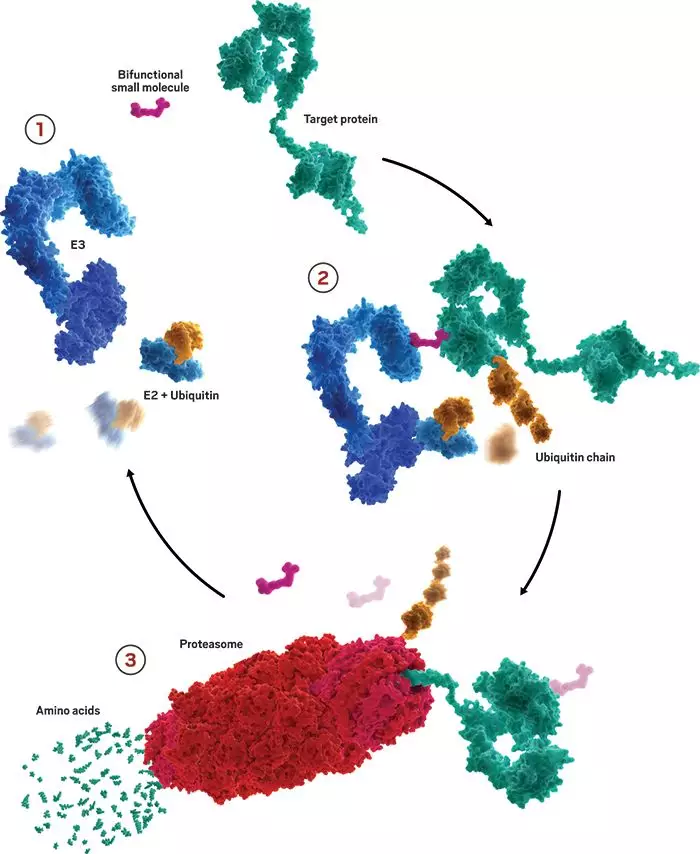
▲蛋白发生降解的过程(图片来源:Kymera Therapeutics)
实际上,降解蛋白质对于疾病治疗有着非常重要的意义——很多严重疾病的背后原因,正是蛋白质的功能失调。但是,常规的小分子药物和抗体类药物只能抑制大约20%的蛋白,剩下的80%被贴上了“不可成药”的标签。而蛋白降解疗法的出现有望攻克这一难题。
靶向蛋白降解剂的设计和优势
人体内的“泛素/E3泛素连接酶”系统是维持蛋白生成和降解平衡的天然系统,负责启动对调节功能异常、折叠或合成错误蛋白的销毁。通常小分子抑制剂想要发挥作用,需要阻断催化位点或者与能够影响蛋白功能的“口袋”相结合。与之不同的是,靶向蛋白降解剂理论上可以与蛋白上的任何角落结合来驱动对蛋白的降解。
靶向蛋白降解剂的设计理念是,通过一种像“双面胶”似的具有两个活性端的小分子,一端与靶标蛋白相结合,另一端与E3泛素连接酶相结合。通过此靶标蛋白会被泛素化,然后被运送到细胞的“垃圾处理站”蛋白酶体中被降解掉。
研究表明,靶标、降解剂和E3连接酶之间构成的三元结构对蛋白降解疗法的疗效非常重要。这个结构最微小的改变可能会影响药物的作用方式。这可以解释为什么有些特异性很差的靶标结合配体转化为降解剂时却表现出了超强的特异性,而有些情况下对任一部件的微小改变却能够将蛋白降解剂的活性完全消除。
与传统疗法相比,靶向蛋白降解剂具有以下几个潜在优势:
理论上,它们具有让原先的“不可成药”靶点成药的潜力,这有望解决各种癌症细胞中约80%的靶点不具有成药性的难题。
蛋白降解剂化合物通常具有很好的可溶性,能够渗透进入细胞,可以口服,并且能够抵抗代谢过程的降解,甚至有些可以跨越血脑屏障,治疗中枢神经系统疾病。
蛋白靶向降解剂在蛋白被降解后,可以被释放出来,继续靶向其它蛋白,从而迅速降低靶向蛋白的水平。这种将药效学和药代动力学分离开的潜力意味着短暂的降解剂作用可能导致对信号通路的长久影响。
新锐领航,技术平台是核心 由于蛋白降解疗法的上述优点,它已成为当下非常有前途的创新疗法之一。目前,许多开发这一创新疗法的新锐公司都获得了资本的青睐。以下,我们将通过几家专注蛋白降解疗法研究的公司,带大家了解下开发这一新疗法的技术平台和在研药物有哪些?
1、Arvinas
Arvinas公司成立于2013年,主要利用蛋白降解平台PROTAC(蛋白降解靶向嵌合体)来开发创新疗法。PROTAC技术使用的是小分子药物,它的一头能靶向目标蛋白,另一头能让E3连接酶与目标蛋白接触促进它降解。通过这种方法,实现特异性地降解特定致病蛋白的目的。

目前,Arvinas公司有两款进展较快的候选药:一款是ARV-110,能选择性地靶向雄激素受体蛋白使其发生降解,拟用于治疗前列腺癌,已被美国FDA授予快速通道资格,该药是首款进入临床的PROTAC小分子药物;另一款是ARV-471,它是靶向雌激素受体(ER)PROTAC蛋白降解剂,拟用于治疗乳腺癌。根据Arvinas公司在去年10月发布的1期临床试验初步结果,这两款在研药均有良好的耐受性。在今年的ASCO年会上,Arvinas公司将公布ARV-110在1期临床试验中的安全性和初步疗效数据。
此外,还值得一提的是,Arvinas公司的科学创始人Craig Crews博士的研究团队开发出一种名为ENDTAC的靶向蛋白降解技术平台,可将蛋白降解技术扩展到靶向细胞外蛋白,有望进一步扩展这一创新治疗模式的适用范围。
2、Kymera Therapeutics
Kymera公司成立于2016年,专注于利用细胞内的泛素-蛋白酶体系统开发创新疗法。其特有的Pegasus技术平台利用人体的天然蛋白回收机制降解致病蛋白,它能够使用基于小分子药物的方法,去针对那些无法被传统小分子药物所抑制的蛋白。2019年,该公司入选了“生物技术猛公司”榜单。

Kymera在研管线中的一个主要靶点是IRAK4。IRAK4是一种在toll样受体和IL-1受体介导的炎症中起重要作用的蛋白。虽然IRAK4能够被小分子抑制剂靶向,但是Kymera的蛋白降解疗法可以通过降解IRAK4,起到小分子抑制剂无法产生的作用。根据该公司去年6月公布的数据,IRAK4蛋白降解剂KYM-001在治疗携带MYD88基因突变的B细胞淋巴瘤时,将IRAK4水平降低75%,并且在小鼠模型中导致肿瘤消退。该公司正计划在多种自身免疫性疾病、肿瘤等适应症中推进IRAK4降解疗法。
此外,Kymera还在开发针对STAT3的新型蛋白质降解疗法。JAK-STAT通路是人类生物学中得到验证最多的通路之一,但作为关键节点,STAT3的成药性并不好。Kymera找到了一些能够结合STAT3与E3连接酶的小分子,在细胞实验和体内实验中,已证实其可以完全降解掉STAT3蛋白。
3、Nurix Therapeutics公司
Nurix Therapeutics公司具有功能互补的两个专有的泛素/E3泛素连接酶平台:一个是“嵌合靶向分子平台”,利用人体的天然蛋白回收系统来降解导致疾病的蛋白;另一个是“E3泛素连接酶抑制剂”平台,通过抑制E3泛素连接酶阻碍人体的天然蛋白回收系统,进而升高靶向蛋白的水平。今年3月,Nurix公司刚完成1.2亿美元融资,以推进其在研疗法进入临床。

目前,Nurix公司的研发管线中进展较快的有两款产品:一款是以BTK为靶点的嵌合靶向分子,拟用于治疗B细胞恶性肿瘤,该公司希望在年底之前向美国FDA提交该药的IND申请;另一款是口服的CBL-B连接酶抑制剂,可刺激T细胞活化和IL-2分泌,是一种新型的免疫肿瘤药物。这两种候选药物都是基于Nurix的DELigase靶向蛋白调节平台开发,该平台能将DNA编码文库的使用和E3连接酶的扩展集结合起来,实现靶向蛋白调节。
4、C4 Therapeutics
C4 Therapeutics(C4T)由来自哈佛大学和丹娜法伯癌症研究所的科学家共同创建,专注于利用细胞自身蛋白降解机制开发创新疗法。C4T公司的策略是力图优化化合物激活泛素系统的能力,而不只是将靶标和连接酶拉近。该公司开发的名为Degronimid的小分子,一方面可以与靶标蛋白结合,另一方面可以与细胞内的泛素蛋白酶体系统中的蛋白相结合,为靶标蛋白加上泛素的标签,使其最终被蛋白酶体降解。

5、Cedilla Therapeutics
Cedilla公司致力开发能够精确调节关键致病蛋白的下一代靶向癌症疗法。该公司采用一种集成的方法,使用小分子来评估恢复蛋白质稳态的多种机制。2018年,Cedilla已完成了由Third Rock 投资的5600万美元A轮融资。

根据Cedilla公司之前发布的新闻稿,该公司正在采取不同的方法来实现降解蛋白的目标:
第一种是通过小分子与靶蛋白结合引发生物物理变化,从而使蛋白质被降解机器所识别;
第二种方法包含上游调节器,通过小分子靶向一个控制蛋白质稳定性的过程,而并针对蛋白质本身;
第三种被称为“蛋白质孤立(protein orphaning)”,当它与其他蛋白结合时,通过干扰蛋白与蛋白的相互作用来破坏蛋白质的稳定性;
第四种方法是通过大规模蛋白质组学来绘制蛋白质易感性图谱,这使得公司能够在蛋白质组中评估每一种蛋白质,以找出哪些条件可能有利于或阻碍降解,并确定以上三种方法中的哪一种最适合。
目前,Cedilla公司尚未公开披露其研发管线。
罗氏、葛兰素史克等大型药企纷纷加入
除了上述新锐企业外,一些全球性药企也加入了蛋白降解疗法的开发中。诺华(Novartis)已经成功使用分子间胶技术降解超过70种靶点蛋白,在研发管线中有10个研发项目,其中一款蛋白降解疗法已经进入临床开发阶段。赛诺菲(Sanofi)开发的SERD(’859)是一款特异性雌激素受体(ER)靶向蛋白降解剂,拟治疗HR阳性乳腺癌患者, 该候选药已获得FDA授予的快速通道资格。
此外,还有一些全球性药企选择与其它公司合作,来布局这一领域。前述几家专注蛋白降解疗法领域的公司,Kymera、Nurix、Arvinas等等都受到了不同全球性药企的青睐。根据公开信息,罗氏、葛兰素史克(GSK)、默沙东、辉瑞(Pfizer)、拜耳(Bayer)等均已与这些公司达成合作,利用它们的专有技术平台,开发针对不同适应症的创新蛋白降解药物。
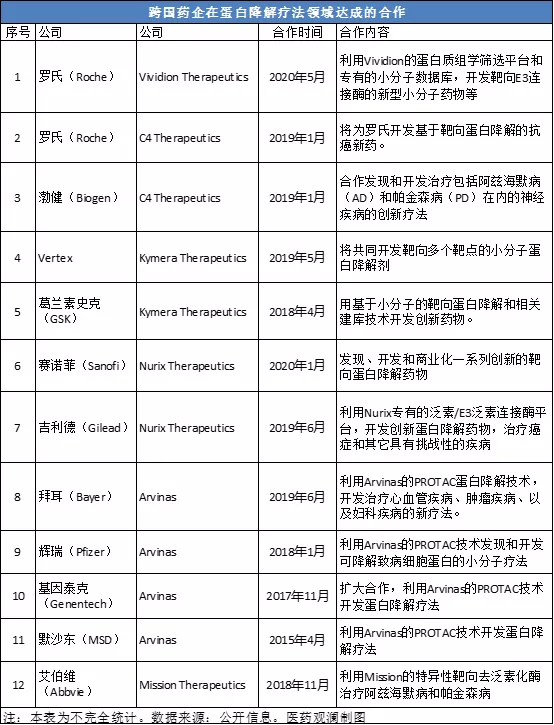
小结
作为一种有望解决80%“不可成药”靶点难题的新型疗法,蛋白降解疗法已被研究人员视为未来人类新药开发最重要的方向之一。目前,拥有蛋白降解疗法开发专有技术的几家新锐公司,不仅得到了资本的看好,也得到了全球性药企的青睐。
在中国,目前开发这一创新疗法的企业并不太多。不过,公开信息显示,已有一些企业涉足这一领域,例如开拓药业开发的雄激素受体(AR)降解剂,目前正处在临床前研究阶段。此外海创药业也拥有开发蛋白降解疗法的PROTAC技术平台。
不过,作为一种新型的技术,蛋白降解疗法的开发过程中还是存在很多挑战。比如一些公司所采用的PROTAC技术,就面临合成路线复杂、步数较多的困难。研究人员也在开发应对这一难关的方法。例如药明康德已经针对PROTAC分子搭建了一个较完善的一体化赋能平台,集发现、合成、分析纯化和测试等能力于一体,可以帮助企业找到更多具有良好药效的PROTAC分子。
最后,希望在科学家、企业、资本等的多方努力下,蛋白降解疗法可以得到快速的发展和进步,攻克“不可成药”靶点的难关,让患者拥有更多的选择!(编辑:任白鸽)






