鼠疫时隔多年再次出现,让人惊恐不已。要知道这种“瘟疫”可比非典、埃博拉病毒厉害的多,以至于卫生机构们都格外小心谨慎。当然,小心之余,艺高人胆大的散户们却在朋友圈中发问,“跪求鼠疫药品概念股”。
智通财经APP也快速翻阅了起治疗药品,均多为抗生素,比如四环素片、盐酸美他环素,以及大输液等。四环素片的生产商就包括上海医药(02607)参股的子公司上海新亚药业;盐酸美他环素则有中国生物制药(01177)的正大天晴(正大丰海)、A股的方盛制药、济川药业等;盐酸多西环素,华润医药(03320)的三九、紫竹都是起生产厂家等;大输液包括华润紫竹、石四药(02005)A股科伦等。
药品概念股不少,但事实上并没有什么炒作价值。相反,这几天公布了自己新药临床数据的华领医药-B(02552)却被二级市场折磨的“痛不欲生”。一天半跌掉了36%,让原本就走的稀稀落落的K线图更加难看。
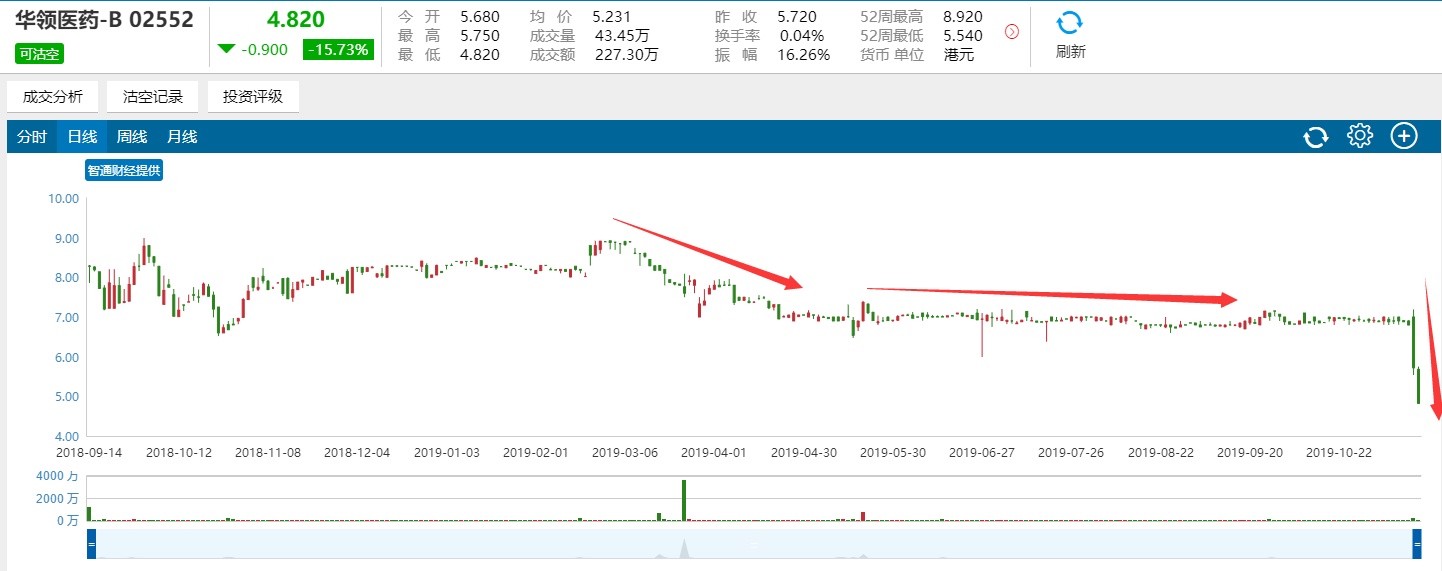
行情来源:智通财经
想颠覆糖尿病奈何现实太无情
说起华领医药,媒体、券商鲜有覆盖,以至于很多人都已经忘记了这位“香港第三只带B”的生物医药公司。
智通财经APP此前在招股书了解到,华领目前致力于开发用于治疗2型糖尿病的全球首创口服新药Dorzagliatin(HMS5552)。资料Dorzagliatin是一种葡萄糖激酶激活剂(或GKA),它通过恢复2型糖尿病患者的葡萄糖稳态平衡来控制糖尿病的渐进性、退行性等特性。
事实上,早期的Dorzagliatin仅仅是一个候选药物,它的由来,还得从全球第一家专注于GKA设计的跨国药企——罗式制药说起。罗氏制药当时研发了第二代GKA药物——Piragliatin,但由于Piragliatin在二期试验中积累了大量人体代谢物,特别是对于定期使用该药物用来治疗2型糖尿病等慢性疾病的患者来说,可能会导致肝脏中毒,因此停止了Piragliatin的进一步研发。
2011年12月,华领医药获罗氏制药授权开发初期候选药物Dorzagliatin。Dorzagliatin是第四代的GKA,专为解决第二代GKA(Piragliatin)的特定缺陷。而根据与罗氏的协议,华领需要向罗氏缴纳各种前期、里程碑及特许权的付款。若华领需要在若干国家或地区提交新药申请,付费最高额达3700万美元;商业化后,若达到特定年度销售额下限后支付款项最高达5500万美元。
所以,华领医药的Dorzagliatin属于典型的授权药。直接点,华领医药不过是罗氏的“打工仔”。
当然,除了罗氏的授权,华领医药也积累了7条研发管线。其中,Dorzagliatin管线、Dorzagliatin与二甲双胍联用的管线均处于临床第三阶段,预计2019年下半年便可完成第三阶段研发,2020年底或2021年上半年之前便可取得新药上市批准。

招股书显示,III期临床试验正在评估Dorzagliatin作为未用药2型糖尿病患者的单药疗法效率,若获国家批准,将成为中国的一线疗法。于此同时,Dorzagliatin与二甲双胍联合使用的效力也正在测评,若获批准,可成为二甲双胍的附加疗法。
华领的产品研发管线还包括Dorzagliatin与其他已获批准的2型糖尿病疗法联用以治疗不同类型的患者。2018年下半年,该公司将开始Dorzagliatin与DPP-4、SGLT-2联合疗法的临床试验,2019年下半年,将开始Dorzagliatin与胰岛素、GLP-1联合疗法的临床试验。
除此之外,该公司还有一条mGLUR5管线,这是一种用于治疗柏金逊病左旋多巴诱导的运动障碍或PD-LID的潜在新型获选药物,公司预计在2019年下半年启动mGLUR5的I期临床试验。
华领将Dorzagliatin与多个已获批治疗药物进行联合试验,是为了生产固定剂量组合药物,以提供个性化的最佳组合疗法。但从另一个角度看,虽然产品组合丰富,但产品类别单一(仅治疗糖尿病患者),若Dorzagliatin最后研发失败,那么余下的5个组合疗法也将“半途而废”,且mGLUR5仍未进入临床试验阶段,单产品类别让风险有所加大。
临床数据爆发力并不惊人
从上述便可以看出Dorzagliatin对华领医药的意义。毫不夸张地说,Dorzagliatin就是华领医药的“全部”。
招股书数据沉浸一年多后,11月11日,智通财经APP观察到,华领医药突然发布公告,称该公司公布全球首创的双重机制葡萄糖激酶启动剂dorzagliatin(HMS5552)的单药治疗III期临床研究(HMM0301,NCT03173391)的24周核心研究结果。

原本一则有望复制长江生命科技(00775)“壮举”的公告,却败给了数据。
按公告透露,Dorzagliatin单药治疗3期注册临床研究(HMM0301)24周核心资料结果,达到研究主要疗效终点;首次开展:针对2型糖尿病病因、专注修复血糖传感葡萄糖激酶、重塑血糖稳态的3期注册临床研究;安全和耐受性好:dorzagliatin治疗24周期间低血糖发生率低于百分之一,无药物相关的严重不良事件发生;疗效显著:dorzagliatin治疗24周后糖化血红蛋白相对基线降低1.07%,显著优于安慰剂,p值小于0.0001;首次实现:由中国创新生物技术公司研发的全球首创2型糖尿病新药达到主要疗效终点。
又是达到研究主要疗效终点,又是安全和耐受性好,又是疗效显著,可为什么就是激不起投资者的爱,反而是被无情的“抛杀呢?这就不得不从28周的观察期,优于安慰剂等数据来说了。
智通财经APP从药物学角度来看,28周的观察期并没有不妥,无非是开放式活性药物治疗的药物安全性研究,让病患自己调节、做好坚持,但7个月“摆脱”医生,能否实现设定要求,这就存在一定变量。另外,就算通过设定临床,7个月后再提交NDA(药品批产上市前的最后考验)对投资者而言等待时间过长。
另外,华领医药公布的疗效显著其实只是优于安慰剂。Dorzagliatin治疗组的糖化血红蛋白(HbA1c)从基线8.35%降低了1.07%(最小二乘法平均值),安慰剂组从基线8.37%降低了0.5%。Dorzagliatin治疗组HbA1c降低与安慰剂组相比,组间差异具有显著的统计学意义(p<0.0001)。针对符合方案资料集的分析结果显示,按照美国糖尿病协会ADA的治疗达标标准(治疗后HbA1c低于7%),dorzagliatin治疗组45.5%的患者达标,对比安慰剂组21.5%达成率,组间差异具有显著的统计学意义(PPS,p<0.0001);血糖稳态控制率复合终点,即HbA1c治疗达标且同时无低血糖事件发生,在dorzagliatin组达到45%,显著高于安慰剂组21.5%达成率(p<0.0001)。
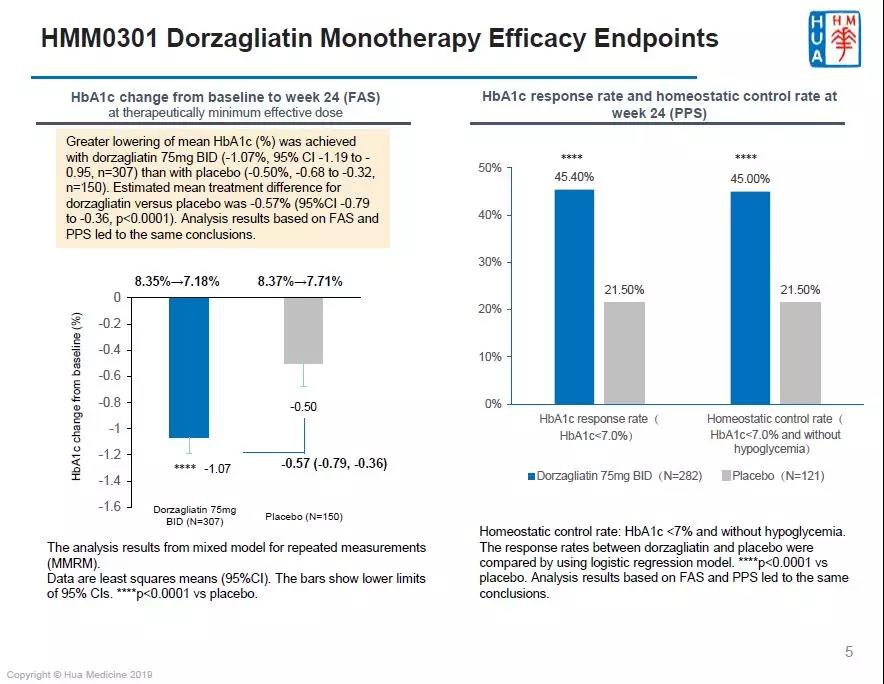
放眼望去,用Dorzagliatin后糖化血红蛋白下降,但达标率50%都不到,根本谈不是上大进步。并且可不要忘记在萄糖激酶激活剂中,近几年国内外企业纷纷加入研发大军,赛道拥挤异常,华领医药的数据仅仅只是好于安慰剂,显然无法取代或威胁当前的如二甲双胍等药品的地位。
所以,华领医药的“大炸弹”目前来看威力并不惊人,前途充满变量。(田宇轩/文)





