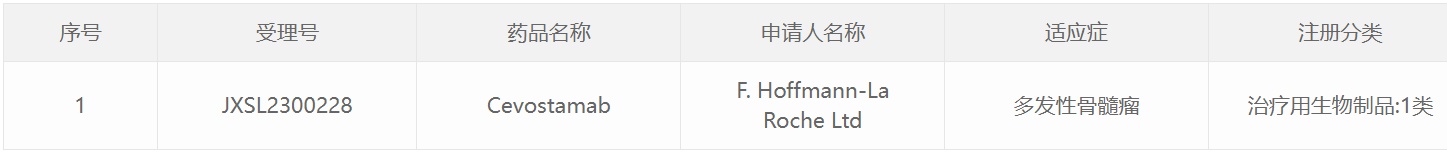
智通财经APP获悉,2月28日,中国国家药监局药品审评中心(CDE)官网公示,罗氏(Roche)(RHHBY.US)申报的1类新药cevostamab获批临床,拟开发治疗多发性骨髓瘤。根据罗氏公开资料,cevostamab(RG6160)是该公司在研的一款双特异性抗体,靶向在骨髓瘤细胞上表达的Fc受体样蛋白5(FcRH5)和T细胞上的CD3。
多发性骨髓瘤(MM)是一种无法治愈的血癌,可影响一种称为浆细胞的白细胞,浆细胞存在于骨髓中。根据罗氏在2021年美国血液学年会(ASH)年会中公布的临床试验结果摘要,截至2021年5月18日,160例接受过多种前期治疗的RRMM患者接受了不同剂量的cevostamab的治疗。
ClinicalTrials平台信息显示,罗氏正在进行多项1/2期临床研究,评估cevostamab单药或联合疗法治疗RRMM患者的疗效和安全性,这些患者在经历抗BCMA治疗等多重治疗后疾病发生进展。





